题目内容
 1L某混合溶液,可能含有的离子如下表:
1L某混合溶液,可能含有的离子如下表:| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH
| ||||
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO
|
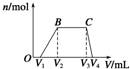
(2)BC段离子方程式为
(3)V1、V2、V3、V4之间的关系为
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:往该溶液中逐滴加入NaOH溶液,开始产生沉淀的物质的量为0,故一定含有H+,那么一定不能含有CO
、AlO
,V1-V2段生成沉淀,且沉淀在V3-V4段全部溶解,故溶液中一定含有Al3+,一定不能含有Mg2+、Fe2+、Fe3+,V2-V3段出现沉淀不减少,但是消耗NaOH溶液,故一定含有NH
,据此分析解答即可.
2- 3 |
- 2 |
+ 4 |
解答:
解:(1)依据分析得出一定不存在的离子是:Mg2+、CO
、AlO
、Fe2+、Fe3+,故答案为:Mg2+、CO
、AlO
、Fe2+、Fe3+;
(2)BC段为铵根与氢氧根反应生成一水合氨的反应,离子反应方程式为:NH 4++OH-=NH3?H2O,故答案为:NH 4++OH-=NH3?H2O;
(3)依据离子反应方程式:Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO 2-+2H2O,即生成氢氧化铝沉淀需要的氢氧化钠是沉淀溶解需要氢氧化钠的3倍,即V2-V1=3(V4-V3),故答案为:V2-V1=3(V4-V3).
2- 3 |
- 2 |
2- 3 |
- 2 |
(2)BC段为铵根与氢氧根反应生成一水合氨的反应,离子反应方程式为:NH 4++OH-=NH3?H2O,故答案为:NH 4++OH-=NH3?H2O;
(3)依据离子反应方程式:Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO 2-+2H2O,即生成氢氧化铝沉淀需要的氢氧化钠是沉淀溶解需要氢氧化钠的3倍,即V2-V1=3(V4-V3),故答案为:V2-V1=3(V4-V3).
点评:本题主要考查的是常见阳离子的检验与铝的化合物的知识,属于高考高频考题,注意总结.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各组物质中,所含分子数相同的是 ( )
| A、10gH2和10gO2 |
| B、5.6LN2和11gCO2 |
| C、9g H2O和0.5mol Cl2 |
| D、标准状况下224mlH2和0.1mol N2 |
2011年11月3日我国自主研制的天宫一号目标飞行器与神舟八号飞船成功实现首次交会对接,标志着我国的载人航天事业进入了一个新的高度.这次任务中的天地话音系统是新研制的设备,由于采用光纤传输取代了以前使用的无线传输,从而避免了多径效应干扰,使得待发段的语音和画面质量更加清晰.光纤的主要成分中含有硅元素,下列关于28Si、29Si、30Si的说法中正确的是( )
| A、28Si、29Si、30Si 是不同元素的三种原子 |
| B、28Si、29Si、30Si 互称为同位素 |
| C、28Si、29Si、30Si 分别含有14、15、16个质子 |
| D、28Si、29Si、30Si都含有14个中子 |
向一定量Fe、FeO、Fe2O3的混合物中加入1 000mL 0.1mol?L-1的盐酸,恰好完全溶解,所得溶液中加KSCN无红色出现,若用足量CO还原相同质量的此混合物,能得到铁( )
| A、11.2 g |
| B、2.8 g |
| C、5.6 g |
| D、无法计算 |
在下列溶液中,各组离子一定能大量共存的是( )
| A、pH=1的溶液中:Na+、Mg2+、SO42-、HCO3- |
| B、含有大量Fe3+的溶液中:Al3+、Cu2+、SO42-、Cl- |
| C、加入A1能放出H2的溶液中:K+、NH4+、NO3-、Cl- |
| D、能使甲基橙呈红色的溶液中:Na+、AlO2-、NO3-、HCO3- |
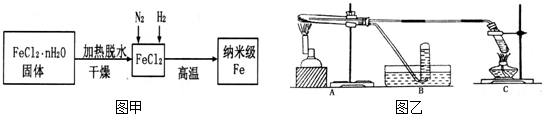
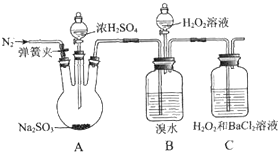 为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).
为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).