题目内容
在下列溶液中,各组离子一定能大量共存的是( )
| A、pH=1的溶液中:Na+、Mg2+、SO42-、HCO3- |
| B、含有大量Fe3+的溶液中:Al3+、Cu2+、SO42-、Cl- |
| C、加入A1能放出H2的溶液中:K+、NH4+、NO3-、Cl- |
| D、能使甲基橙呈红色的溶液中:Na+、AlO2-、NO3-、HCO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.pH=1的溶液呈酸性;
B.如离子之间不发生任何反应,则可大量共存;
C.加入A1能放出H2的溶液可能呈强碱性,或为非氧化性酸溶液;
D.能使甲基橙呈红色的溶液呈酸性.
B.如离子之间不发生任何反应,则可大量共存;
C.加入A1能放出H2的溶液可能呈强碱性,或为非氧化性酸溶液;
D.能使甲基橙呈红色的溶液呈酸性.
解答:
解:A.PH=1的溶液呈酸性,酸性条件下HCO3-不能大量共存,故A错误;
B.离子之间不发生任何反应,可大量共存,故B正确;
C.加入A1能放出H2的溶液可能呈强碱性,或为非氧化性酸溶液,碱性条件下NH4+不能大量共存,酸性条件下NO3-不能大量共存,故C错误;
D.能使甲基橙呈红色的溶液呈酸性,酸性条件下AlO2-、HCO3-不能大量共存,且而发生反应,故D错误.
故选B.
B.离子之间不发生任何反应,可大量共存,故B正确;
C.加入A1能放出H2的溶液可能呈强碱性,或为非氧化性酸溶液,碱性条件下NH4+不能大量共存,酸性条件下NO3-不能大量共存,故C错误;
D.能使甲基橙呈红色的溶液呈酸性,酸性条件下AlO2-、HCO3-不能大量共存,且而发生反应,故D错误.
故选B.
点评:本题考查了离子共存,为高考常见题型,侧重于学生的分析能力的考查,题目难度中等,注意明确离子反应发生条件,掌握常见的离子不能共存的情况,特别注意发生氧化还原反应的离子.

练习册系列答案
相关题目
化学实验要注意安全,符合安全要求的是( )
| A、凡是给玻璃仪器加热时,都要加垫石棉网,以防仪器炸裂 |
| B、稀释浓硫酸时,将水倒入浓硫酸中 |
| C、浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 |
| D、浓硫酸溅到皮肤上,立即用稀NaOH溶液洗涤 |
“类推”是常用的学习方法,但有时会产生错误结论,下列类推的结论中,正确的是( )
| A、ⅣA族元素氢化物沸点顺序是:GeH4>SiH4>CH4,则V A族元素氢化物沸点顺序也是:AsH3>PH3>NH3 |
| B、第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3,则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
| C、存在离子键的化合物是离子化合物,则存在共价键的是共价化合物 |
| D、KNO3溶于水时溶液温度无明显变化,则NH4NO3溶于水时溶液温度也无明显变化 |
实验室对某有机物有如下实验记录:①在O2中充分燃烧,只生成CO2和H2O;②完全燃烧0.1mol该有机物需消耗标准状况下11.2LO2.4位同学据此分别提出以下4种该有机物可能的分子式,其中合理的是( )
| A、C2H6 |
| B、C3H10O |
| C、C4H8O2 |
| D、C5H10O3 |
今有一混合无色澄清的水溶液,只可能含有以下离子中的若干种:Cu2+、NH4+、Cl-、
Ca2+、Ba2+、K+、CO32-、SO42-,现取三份10mL溶液进行如下实验:
①第一份加入AgNO3溶液有白色沉淀产生
②第二份加足量NaOH溶液,加热后会收集到气体
③第三份加足量BaCl2溶液后,得沉淀6.27g,经足量盐酸洗涤、干燥,沉淀质量为2,.33g.根据上述实验,以下推测正确的是( )
Ca2+、Ba2+、K+、CO32-、SO42-,现取三份10mL溶液进行如下实验:
①第一份加入AgNO3溶液有白色沉淀产生
②第二份加足量NaOH溶液,加热后会收集到气体
③第三份加足量BaCl2溶液后,得沉淀6.27g,经足量盐酸洗涤、干燥,沉淀质量为2,.33g.根据上述实验,以下推测正确的是( )
| A、NH4+、SO42-一定存在 |
| B、该溶液中含CO32-离子的浓度为1 mol/L |
| C、Cl-一定存在 |
| D、Ba2+一定不存在,Cu2+、Ca2+可能存在 |
下列各组元素中,属于同一周期的是( )
| A、Mg、F | B、N、P |
| C、Al、Si | D、O、Cl |
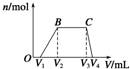 1L某混合溶液,可能含有的离子如下表:
1L某混合溶液,可能含有的离子如下表: