题目内容
16.将10.7g Mg、Al和Fe组成的合金溶于足量的氢氧化钠溶液中,产生标准状况下4.48L 气体,另取等质量的合金溶于过量盐酸中,生成标准状况下7.84L气体,向反应后的溶液加入过量NaOH溶液,得到沉淀物质的量为( )| A. | 0.1mol | B. | 0.15mol | C. | 0.25mol | D. | 0.3mol |
分析 Mg、Al和Fe组成的合金溶于足量的氢氧化钠溶液中,只有Al反应生成氢气,根据电子转移守恒计算Al提供电子物质的量.另取等质量的合金溶于过量盐酸中,金属均与盐酸反应生成氢气,两过程中Al反应生成氢气体积相等,根据电子转移守恒计算Mg、Fe总物质的量,向反应后的溶液中加入过量NaOH溶液,得到沉淀为氢氧化镁、氢氧化亚铁,根据原子守恒计算沉淀物质的量.
解答 解:Mg、Al和Fe组成的合金溶于足量的氢氧化钠溶液中,只有Al反应生成氢气,根据电子转移守恒,Al提供电子物质的量为:$\frac{4.48L}{22.4L/mol}$×3=0.6mol;
另取等质量的合金溶于过量盐酸中,金属均与盐酸反应生成氢气,两过程中Al反应生成氢气体积相等,根据电子转移守恒,Mg、Fe提供电子总物质的量为:$\frac{7.84g}{22.4L/mol}$×2-0.4mol=0.3mol,故Mg、Fe总物质的量为:$\frac{0.3mol}{2}$=0.15mol,
向反应后的溶液中加入过量NaOH溶液,得到沉淀为氢氧化镁、氢氧化亚铁,
根据原子守恒,沉淀物质的量等于金属物质的量,则生成沉淀物质的量为0.15mol,
故选B.
点评 本题混合物反应的有关计算,题目难度中等,明确发生反应的实质为解答关键,注意从守恒的角度进行解答,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
7.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 将1mol铁粉加入到一定量的稀硝酸溶液中充分反应,转移的电子数一定是3NA | |
| B. | 标准状况下,22.4L己烷中共价键数目为19NA | |
| C. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA | |
| D. | 1.0 L 1.0 mol•L-1 NaClO溶液中含有ClO-离子的数目为NA |
4.下列有机物中,既能发生消去反应,又能发生酯化反应,还能发生催化氧化,且催化氧化产物能发生银镜反应的是( )
| A. | CH3OH | B. | CH3CH(OH)COOH | C. | (CH3)2C(OH)CH2CH3 | D. | HOCH2CH2COOH |
11.下列反应中,SO2作还原剂的是( )
| A. | 2H2S+SO2═3S↓+2H2O | B. | Cl2+SO2+2H2O═H2SO4+2HCl | ||
| C. | SO2+2Mg═2MgO+S | D. | SO2+2NaOH═Na2SO3+H2O |
1.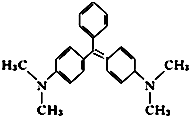 孔雀石绿是化工产品,具有较高毒性,高残留,容易致癌、致畸. 其结构简式如图所示.下列关于孔雀石绿的说法正确的是( )
孔雀石绿是化工产品,具有较高毒性,高残留,容易致癌、致畸. 其结构简式如图所示.下列关于孔雀石绿的说法正确的是( )
 孔雀石绿是化工产品,具有较高毒性,高残留,容易致癌、致畸. 其结构简式如图所示.下列关于孔雀石绿的说法正确的是( )
孔雀石绿是化工产品,具有较高毒性,高残留,容易致癌、致畸. 其结构简式如图所示.下列关于孔雀石绿的说法正确的是( )| A. | 孔雀石绿的分子式为C23H25N2 | |
| B. | 孔雀石绿属于芳香烃 | |
| C. | 孔雀石绿苯环上的一氯取代物有5种 | |
| D. | 1mol孔雀石绿在一定条件下最多可与6 mol H2发生加成反应 |
8.品红分子结构中的发色基团遇到SO2与水形成的亚硫酸后结构发生改变,生成不稳定的无色化合物.亚硫酸漂白原理可用下面的反应方程式表示下列说法不正确的是( )


| A. | 品红的分子式为C20H19N3 | |
| B. | 上述漂白原理反应属加成反应 | |
| C. | 碱性品红及其与H2SO3生成的无色化合物都可与NaOH溶液反应 | |
| D. | 碱性品红与H2SO3生成的无色化合物不稳定,加热后恢复原来的颜色 |
5.标准状况下,将5.6L由CO、CH4、C2H4、C2H2组成的混合气体与18LO2混合于某密闭容器中点燃,反应完成后再恢复到原状况,得CO2气体7.50L,则下列判断正确的是( )
| A. | 反应完成后,O2有剩余 | |
| B. | 原混合气体中,C2H4与C2H2的体积共为1.9L | |
| C. | 反应完成后,生成水的质量为9g | |
| D. | 原混合气体中,CO与CH4的体积比一定为1:1 |
19.影响化学反应速率的主要因素是( )
| A. | 温度 | B. | 催化剂 | C. | 物质的性质 | D. | 浓度 |