题目内容
4.下列说法或解释正确的是( )| A. | 硅胶作干燥剂是利用其多孔、吸附水分的能力强 | |
| B. | 铝在空气中必须出良好的抗腐蚀性,说明铝极难与氧气反应 | |
| C. | 明矾可用于饮水的消毒杀菌 | |
| D. | 光导纤维比普通电缆有更强的传输信息能力,是因为其导电能力强 |
分析 A.硅胶是硅酸的冻状凝结经脱水后得到的,多孔、吸附水分的能力强;
B.铝极易与空气的氧气反应生成致密的氧化铝薄膜,阻止了内层铝继续被氧化;
C.氢氧化铝胶体具有吸附性而净水;
D.光导纤维的成分是二氧化硅,不能导电;
解答 解:A.硅胶是硅酸的冻状凝结经脱水后得到的,多孔,吸附水分能力强,常用作袋装食品、瓶装药品的干燥剂,故A正确;
B.铝属于活泼金属,极易与空气的氧气反应生成致密的氧化铝薄膜,阻止了内层铝继续被氧化,故表现出抗腐蚀性,故B错误;
C.明矾可以用于水的净化,原理是铝离子水解生成的氢氧化铝胶体能吸附水中的悬浮物质而净水,明矾不能杀菌、消毒,故C错误;
D.光导纤维传输信号是利用光的全反射现象传输信息,所以大量用于制造通信光缆,但是不导电,故D错误;
故选A.
点评 本题是一道化学和生活相联系的知识,掌握硅胶、铝、明矾、二氧化硅的性质是解答关键,题目难度不大.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
15.分子式为CxHyO2的有机物1mol在氧气中燃烧,产生二氧化碳和水蒸气的体积相等,并耗氧气3.5mol,则该有机物中x、y的值分别为( )
| A. | 1、2 | B. | 2、3 | C. | 3、6 | D. | 4、6 |
12.下列说法不正确的是( )
| A. | 用干燥洁净的玻璃棒蘸取NaClO溶液,滴到放在表面皿上的pH试纸上测pH | |
| B. | 实验时受溴腐蚀致伤,先用苯或甘油洗伤口,再用水洗 | |
| C. | 可用重结晶法提纯含少量NaCl的KNO3晶体 | |
| D. | 容量瓶、滴定管上都标有使用温度,容量瓶无“O”刻度,滴定管有“O”刻度,使用前水洗后滴定管还需润洗,而容量瓶不需要润洗 |
19.W、X、Y、Z均是短周期元素,W元素原子的最外层电子数与次外层电子数之差的绝对值等于其电子层数,X元素的原子比W元素的原子多2个电子;Y+和Z-离子具有与氖原子相同的电子层结构.下列说法错误的是( )
| A. | 上述元素中,Y的原子半径最大 | |
| B. | 上述元素中,W的气态氢化物最稳定 | |
| C. | 元素W和X可形成含有极性键的极性分子WX3 | |
| D. | 工业上可用电解熔融的Y、Z的化合物的方法冶炼Y、Z的单质 |
9.下列说法不正确的是( )
| A. | 二氯丙烷有三种同分异构体 | |
| B. | 碳酸氢钠可用作食品加工中的无铝发泡剂,快速发酵粉 | |
| C. | 二氧化碳制全降解塑料有助于控制温室效应和白色污染 | |
| D. | 某化合物的分子式为C8H10O,其中能与乙酸发生酯化反应的同分异构体有4种 |
16.下列化学用语表达正确的有( )
①羟基的电子式: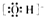
②次氯酸分子的结构式:H-O-Cl
③乙烯的最简式(实验式):CH2=CH2
④含有10个中子的氧原子:188O
⑤铝离子的结构示意图: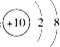
⑥二氧化碳分子的比例模型
①羟基的电子式:
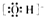
②次氯酸分子的结构式:H-O-Cl
③乙烯的最简式(实验式):CH2=CH2
④含有10个中子的氧原子:188O
⑤铝离子的结构示意图:
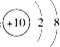
⑥二氧化碳分子的比例模型

| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
14.某温度T1时,向容积为2L的恒容密闭容器中充入一定量的H2和I2(g),发生反应:H2(g)+I2(g)?2HI(g)反应过程中测定的部分数据见下表(表中t2>t1):下列说法正确的是( )
| 反应时间/min | n(H2)/mol | n(I2)/mol |
| 0 | 0.9 | 0.3 |
| t1 | 0.8 | |
| t2 | 0.2 |
| A. | 反应在t1 min内的平均速率为:v(H2)=$\frac{0.1}{{t}_{1}}$mol•L-1•min-1 | |
| B. | 保持其他条件不变,向平衡体系中再通入0.20 mol H2,与原平衡相比,达到新平衡时I2(g)转化率增大,H2的体积分数不变 | |
| C. | 保持其他条件不变,起始时向容器中充入的H2和I2(g)都为0.5mol,达到平衡时n(HI)=0.2 mol | |
| D. | 升高温度至T2时,上述反应平衡常数为0.18,则正反应为吸热反应 |
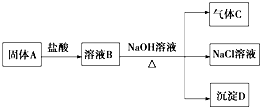
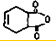 一种生产除虫剂胺菊酯的重要原料,其合成路线如下:
一种生产除虫剂胺菊酯的重要原料,其合成路线如下: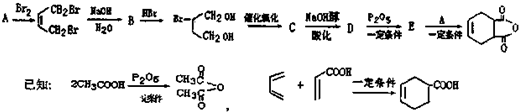
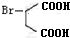 ,A的系统命名为1,3-丁二烯;
,A的系统命名为1,3-丁二烯; ;
;