题目内容
8.一块表面已部分被氧化的钠,质量为10.8克,将其放入100ml水中,可收集到标准状况下2.24L气体,则钠元素的质量分数为?分析 根据n=$\frac{V}{{V}_{m}}$计算氢气的物质的量,再根据反应2Na+2H2O=2NaOH+H2↑计算样品中Na的质量,进而计算Na2O的质量,根据Na2O中元素质量分数计算含有Na元素的质量,最后根据总质量计算出钠元素的质量分数.
解答 解:生成的气体为氢气,其物质的量为:n(H2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,
2Na+2H2O=2NaOH+H2↑
46g 1mol
m(Na) 0.1mol
m(Na)=$\frac{46g×0.1mol}{1mol}$=4.6g,
故10.8g样品中含有氧化钠的质量为:m(Na2O)=10.8g-4.6g=6.2g,
Na2O中Na元素的质量为:6.2g×$\frac{46}{62}$=4.6g,
所以样品中钠元素的质量分数为:$\frac{4.6g+4.6g}{10.8g}$×100%≈85.2%,
答:该样品中钠元素的质量分数为85.2%.
点评 本题考查了化学方程式的有关计算,题目难度中等,明确发生反应的原理为解答关键,注意掌握质量守恒在化学计算中的应用,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.将0.4mol/L的NH4Cl溶液与0.2mol/L的NaOH溶液等体积混合,则混合溶液中下列离子的浓度关系正确的是( )
| A. | c ( NH4+)+c ( Na+)=c ( Cl-)+c ( OH-) | |
| B. | c ( NH4+)+c ( NH3•H2O )=0.4mol/L | |
| C. | c ( Cl-)>c ( NH4+)>c ( Na+)>c ( OH-)>c ( H+) | |
| D. | c ( Cl-)>c ( Na+)>c ( NH4+)>c ( H+ )>c ( OH-) |
19.向甲溶液中缓慢滴加乙溶液,反应生成沉淀的质量与乙溶液的量之间的关系如图所示,其中符合图象的是( )
| 甲 | 乙 | 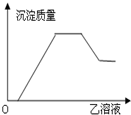 | |
| A | AlCl3、Mg(NO3)2、HNO3 | NaOH | |
| B | Na2CO3、NH4HCO3、Na2SO4 | Ba(OH)2 | |
| C | NH4NO3、Al(NO3)3、Fe(NO3)3、HCl | NaOH | |
| D | NaAlO2、氨水、NaOH | H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
16.下列金属单质能与硫酸铜溶液反应且不产生气体的是( )
| A. | 金 | B. | 银 | C. | 钠 | D. | 镁 |
3.下列说法正确的是( )
| A. | C60的摩尔质量是720 | |
| B. | 金刚石、石墨和C60互为同位素 | |
| C. | 因石墨具有导电性,可用石墨炸弹破坏输电线、电厂设备 | |
| D. | 在点燃的条件下,碳可以还原氧化镁生成镁和二氧化碳 |
20.300℃时,将100mL由H2O、CO2和N2组成的混合气体通入盛有足量Na2O2的密闭容器中(容器体积保持不变),充分反应后恢复到原温度时容器内的压强变为原来的$\frac{4}{5}$.则原混合气体中N2的体积分数为( )
| A. | 33.3% | B. | 40% | C. | 60% | D. | 75% |
18.下列反应中的氨与反应4NH3+5O2→4NO+6H2O中的氨作用相同的是( )
| A. | 2NH3+3CuO→3Cu+N2+3H2O | B. | 2Na+2NH3→2NaNH2+H2↑ | ||
| C. | 4NH3+6NO→5N2+6H2O | D. | 3SiH4+4NH3→Si3N4+12H2 |
