题目内容
5.固体X只可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的一种或几种组成,某同学对该固体进行了如下实验,下列判断正确的是( )
| A. | 白色沉淀乙不一定是Al(OH)3 | B. | 气体甲一定是纯净物 | ||
| C. | 固体X中一定存在(NH4)2SO4、MgCl2 | D. | 固体X中一定存在FeCl2、AlCl3 |
分析 固体X只可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的一种或几种组成,X中加入过量Ba(OH)2溶液并加热,产生气体甲,甲能使湿润的红色石蕊试纸变蓝色,说明甲中含有NH3,Al也能和NaOH反应生成氢气,所以甲可能是NH3也可能是H2和NH3,则X中一定含有(NH4)2SO4;产生白色沉淀甲,且沉淀甲久置没有明显变化,所以白色沉淀不是Fe(OH)2,则溶液中不存在FeCl2,生成的沉淀白色沉淀甲是BaSO4或BaSO4和Mg(OH)2的混合物,所以X中可能含有MgCl2;
无色溶液甲中通入二氧化碳生成白色沉淀乙和无色溶液乙,因为加入的Ba(OH)2是过量的,白色沉淀乙能溶于稀盐酸,所以生成的白色沉淀乙可能是BaCO3或Al(OH)3和BaCO3的混合物,则X中可能含有AlCl3;
据此分析解答.
解答 解:固体X只可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的一种或几种组成,X中加入过量Ba(OH)2溶液并加热,产生气体甲,甲能使湿润的红色石蕊试纸变蓝色,说明甲中含有NH3,Al也能和NaOH反应生成氢气,所以甲可能是NH3也可能是H2和NH3,则X中一定含有(NH4)2SO4;产生白色沉淀甲,且沉淀甲久置没有明显变化,所以白色沉淀不是Fe(OH)2,则溶液中不存在FeCl2,生成的沉淀白色沉淀甲是BaSO4或BaSO4和Mg(OH)2的混合物,所以X中可能含有MgCl2;无色溶液甲中通入二氧化碳生成白色沉淀乙和无色溶液乙,因为加入的Ba(OH)2是过量的,白色沉淀乙能溶于稀盐酸,所以生成的白色沉淀乙可能是BaCO3或Al(OH)3和BaCO3的混合物,则X中可能含有AlCl3;
A.通过以上分析知,白色固体乙可能是BaCO3或Al(OH)3和BaCO3的混合物,所以白色沉淀乙不一定是Al(OH)3,故A正确;
B.通过以上分析知,气体甲可能是NH3也可能是H2和NH3,所以甲不一定是纯净物,故B错误;
C.通过以上分析知,X中一定含有(NH4)2SO4,可能含有MgCl2、AlCl3,故C错误;
D.固体X中一定不存在FeCl2,可能含有AlCl3,故D错误;
故选A.
点评 本题考查物质检验和鉴别,为高频考点,明确物质性质及物质之间转化是解本题关键,熟练掌握物质之间的反应,侧重考查学生分析判断及思维缜密性,题目难度中等.

| A. | 6和8 | B. | 11和8 | C. | 20和8 | D. | 20和17 |
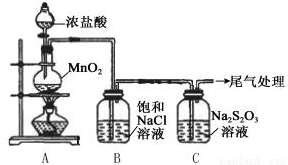
实验操作和现象:
| 操作 | 现象 |
| 打开分液漏斗活塞,滴加一定量浓盐酸,加热 | i.A中有黄绿色气体生成,C中液面上方有白雾,溶液中开始出现少量浑浊; ii.一段时间后,C中产生大量黄色沉淀. |
| 用湿润的淀粉碘化钾试纸检验C中白雾 | 淀粉碘化钾试纸变蓝 |
| C中浊液过滤后,取少量滤液用盐酸酸化,滴加氯化钡溶液 | 有白色沉淀生成 |
(2)B中饱和NaCl溶液的作用是除去Cl2中的HCl,防止对Cl2与Na2S2O3的反应产生干扰.
(3)C中生成黄色沉淀的离子方程式是S2O32-+2H+=S↓+SO2↑+H2O.
(4)将C中雾通入品红溶液检验是否有SO2,该操作不合理的理由是C中雾有氯气.
(5)C中滤液与氯化钡溶液反应生成白色沉淀,甲同学认为利用该现象可证明Na2S2O3被Cl2氧化,反应的离子方程式是.乙同学认为,C中滤液用硝酸酸化后滴加硝酸银溶液,若有白色沉淀,也能证明Na2S2O3被Cl2氧化,丙同学认为不能证明,理由是氯气与水反应也能生成Cl-,所以检验出溶液中有Cl-也不能证明是Cl2氧化了Na2S2O3.

| A. | Cu2+物质的量浓度 | B. | Cl-物质的量浓度 | ||
| C. | Cu极质量 | D. | C(石墨)极质量 |
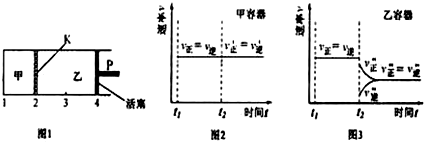
| A. | 保持温度和活塞位置不变,在甲中再加入1molA和2molB,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 | |
| B. | 保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数增大,乙中B的体积分数减小 | |
| C. | 保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 | |
| D. | 保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
| A. | 丙酮与HCN发生加成反应 | |
| B. | 1,3-丁二烯生成 聚1,3-丁二烯 | |
| C. | 乙二醇与重铬酸钾溶液共热被氧化为乙二酸(HOOC-COOH) | |
| D. | 乙苯与酸性高锰酸钾溶液反应 |
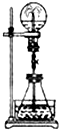 喷泉实验是一种常见的自然现象,其产生原因是存在压强差.在图中的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( )
喷泉实验是一种常见的自然现象,其产生原因是存在压强差.在图中的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( )| A. | Cu与稀盐酸 | B. | NH4HCO3与稀盐酸 | ||
| C. | CaCO3与稀硫酸 | D. | NaHCO3与NaOH溶液 |
 .
. NOx是汽车尾气中的主要污染物之一.通过NOx传感器可监测NOx的含量,其工作原理如图:
NOx是汽车尾气中的主要污染物之一.通过NOx传感器可监测NOx的含量,其工作原理如图: