题目内容
10.①NaOH溶液 ②铜丝 ③液态HCl ④盐酸 ⑤稀硫酸 ⑥液氨 ⑦氨水 ⑧SO2 ⑨胆矾晶体 ⑩熔融NaCl (11)蔗糖晶体 (12)酒精 (13)酒精溶液(1)上述状态下可导电的是①②④⑤⑦⑩;
(2)属于非电解质的是⑥⑧(11)(12);
(3)上述状态下的电解质不能导电的是③⑨.
分析 (1)从电解质导电的状态和金属导电来思考;
(2)非电解质是指在水溶液里和熔化状态下都不能导电的化合物;
(3)根据电解质的概念和导电状态考虑.
解答 解:(1)在NaOH溶液、盐酸、稀硫酸、氨水中存在自由移动的离子而导电,熔融NaCl中存在自由的钠离子和氯离子,能够导电;铜丝属于金属,能够导电;
故答案为:①②④⑤⑦⑩;
(2)非电解质是指在水溶液里和熔化状态下都不能导电的化合物,酒精溶液不导电,酒精属于非电解质;蔗糖溶液不导电,蔗糖属于非电解质;液氨和二氧化硫的水溶液能够导电,是因为它们溶于水分别生成了电解质一水合氨和亚硫酸,不是它们自身原因而导电,即液氨和二氧化硫属于非电解质;
故答案为:⑥⑧(11)(12);
(3)胆矾晶体在水溶液能电离出自由移动的离子而导电,属于电解质,但胆矾晶体中没有自由移动的离子,不能导电;液态HCl在水溶液中能电离出自由移动的离子而导电,但在液态HCl中没有自由移动的离子,不能导电;
故答案为:③⑨.
点评 本题考查了电解质和非电解质的判断及能导电的物质,注意能导电的物质不一定是电解质,电解质不一定导电,为易错点.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
20.用NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,22.4LCHCl3中含有的氯原子的数目为3NA | |
| B. | 25℃、101kPa下,16gO3和O2混合气体中含有的氧原子数为NA | |
| C. | 等质量的N2和CO所含分子数相同且均为NA | |
| D. | 一定温度下,1L 1mol•L-1的CH3COONa溶液含NA个CH3COO- |
1.C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,下列做法不能加快化学反应速率的是( )
| A. | 增大氧气浓度 | B. | 升高反应温度 | C. | 增大木炭的量 | D. | 将炭磨成炭粉 |
2.某中学化学兴趣小组为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量的10%的稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水).有关实验数据如下表:
请计算(写出计算过程):
(1)该石灰石中碳酸钙的质量分数;
(2)参加反应10%的盐酸的质量.
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 134.4 g | 10 g | 141.1 g | |
(1)该石灰石中碳酸钙的质量分数;
(2)参加反应10%的盐酸的质量.
20.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4L H2含有的分子数为NA | |
| B. | 标准状况下,80g SO3的体积为22.4L | |
| C. | 18g H2O在标准状况下的体积是22.4L | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA |
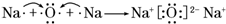 .A、B两种元素还可以形成A2B2型化合物,写出该化合物的电子式
.A、B两种元素还可以形成A2B2型化合物,写出该化合物的电子式 .
.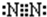 ;
; ;
;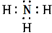 .
.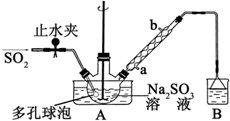 次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)俗称吊白块,不稳定,120℃时会分解.在印染、医药以及原子能工业中有广泛应用.以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如图:
次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)俗称吊白块,不稳定,120℃时会分解.在印染、医药以及原子能工业中有广泛应用.以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如图: