题目内容
20.用NA表示阿伏加德罗常数,下列叙述正确的是( )| A. | 标准状况下,22.4L H2含有的分子数为NA | |
| B. | 标准状况下,80g SO3的体积为22.4L | |
| C. | 18g H2O在标准状况下的体积是22.4L | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA |
分析 A.依据n=$\frac{V}{Vm}$计算氢气的物质的量,依据N=NA•n解答;
B.气体摩尔体积适应对象为气体;
C.标况下水是液体,不能使用气体摩尔体积;
D.溶液体积未知.
解答 解:A.标准状况下,22.4L H2中含氢气的物质的量为$\frac{22.4L}{22.4/mol}$=1mol,分子数为1•NA=NA,故A正确;
B.标况下三氧化硫不是气体,不能使用气体摩尔体积,故B错误;
C.标况下水是液体,不能使用气体摩尔体积,故C错误;
D.溶液体积未知,无法计算氯离子个数,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意气体摩尔体积使用条件和对象,题目难度不大.

练习册系列答案
相关题目
8.在如图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述正确的是( )


| A. | 碳棒上有气体放出,溶液酸性变弱 | |
| B. | a是正极,b是负极 | |
| C. | 导线中有电子流动,电流从a极到b极 | |
| D. | a极上发生了还原反应 |
5.下列关于水的说法正确的是( )
| A. | 纯水几乎不导电,因此水是非电解质 | |
| B. | 在任何温度下,纯水的pH均等于7 | |
| C. | 向水中加入钠,溶液中$\frac{{K}_{w}}{c(O{H}^{-})}$减小 | |
| D. | 向水中加入醋酸,c(H+)和水的电离均增大 |
17. 对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺与浓硫酸(HO-SO3H)磺化得到.实验室可利用右图装置合成对氨基苯磺酸
对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺与浓硫酸(HO-SO3H)磺化得到.实验室可利用右图装置合成对氨基苯磺酸
实验步骤如下:
①在一个250mL三口烧瓶中加入10mL苯胺及少量固体B,把烧瓶放入冷水中,缓慢地加入18mL浓硫酸.
②把三口烧瓶置于油浴中缓慢加热,控制温度为180℃~190℃,反应1~1.5h.
③将反应液冷却至约50℃,倒入盛有100mL冷水的烧杯中,析出灰白色固体,进行操作C并用少量冷水洗涤固体,得到对氨基苯磺酸粗产品.
④对粗产品进行操作D,再低温烘干即得到纯净的对氨基苯甲酸.
以下为两种有机物的部分物理性质,请回答有关问题.
(1)由苯胺生成对氨基苯磺酸的反应方程式为 .
.
(2)装置A的名称为冷凝管,作用是使苯胺冷凝回流.
(3)固体 B的作用是防暴沸,操作C的名称是过滤.
(4)下列说法正确的是AD
A.用液体加热的好处是反应物受热均匀,便于控制温度
B.本实验步骤②也可以改用水浴加热
C.步骤③将反应液倒入100mL冷水的目的是分离苯胺和对氨基苯磺酸
D.步骤③用少量冷水洗涤的目的是除去固体表面的可溶性杂质同时减少洗涤过程中的损失.
(5)操作D的名称是重结晶,具体过程包括:用适量热水溶解粗产品→冷却结晶→过滤、洗涤.
 对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺与浓硫酸(HO-SO3H)磺化得到.实验室可利用右图装置合成对氨基苯磺酸
对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺与浓硫酸(HO-SO3H)磺化得到.实验室可利用右图装置合成对氨基苯磺酸
实验步骤如下:
①在一个250mL三口烧瓶中加入10mL苯胺及少量固体B,把烧瓶放入冷水中,缓慢地加入18mL浓硫酸.
②把三口烧瓶置于油浴中缓慢加热,控制温度为180℃~190℃,反应1~1.5h.
③将反应液冷却至约50℃,倒入盛有100mL冷水的烧杯中,析出灰白色固体,进行操作C并用少量冷水洗涤固体,得到对氨基苯磺酸粗产品.
④对粗产品进行操作D,再低温烘干即得到纯净的对氨基苯甲酸.
以下为两种有机物的部分物理性质,请回答有关问题.
| 苯胺 | 对氨基苯磺酸 | |
| 熔点 | -6.3℃ | 288℃ |
| 沸点 | 184℃ | (300℃开始分解炭化) |
| 水溶性 | 微溶于水 | 微溶于冷水、溶于热水 |
 .
.(2)装置A的名称为冷凝管,作用是使苯胺冷凝回流.
(3)固体 B的作用是防暴沸,操作C的名称是过滤.
(4)下列说法正确的是AD
A.用液体加热的好处是反应物受热均匀,便于控制温度
B.本实验步骤②也可以改用水浴加热
C.步骤③将反应液倒入100mL冷水的目的是分离苯胺和对氨基苯磺酸
D.步骤③用少量冷水洗涤的目的是除去固体表面的可溶性杂质同时减少洗涤过程中的损失.
(5)操作D的名称是重结晶,具体过程包括:用适量热水溶解粗产品→冷却结晶→过滤、洗涤.
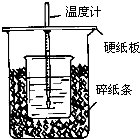 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: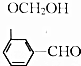


 某化学课外兴趣小组学生用如图所示的装置探究苯和液溴的反应并制备溴苯.请分析后回答下列问题:
某化学课外兴趣小组学生用如图所示的装置探究苯和液溴的反应并制备溴苯.请分析后回答下列问题: .
.