题目内容
1.某微粒的结构示意图为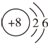 ,该微粒是元素周期表中的氧元素,它的核电荷数是8,碳元素的核电荷数是6,由此可知不同元素的本质区别是质子数不同.
,该微粒是元素周期表中的氧元素,它的核电荷数是8,碳元素的核电荷数是6,由此可知不同元素的本质区别是质子数不同.
分析 根据该微粒的结构示意图可知,此微粒的质子数和电子数相同,故此微粒为原子,根据质子数为8可知此原子的种类;核电荷数即原子核所带的电荷数;由于核电荷数=原子序数,而碳元素为6号元素,据此分析核电荷数;元素是具有相同质子数的同一类原子的总称.
解答 解:根据该微粒的结构示意图可知,此微粒的质子数和电子数相同,均为8个,故此微粒为原子,根据此原子的质子数为8,可知此微粒为O原子,故为氧元素;核电荷数即原子核所带的电荷数,根据示意图可知,其核电荷数为8;由于核电荷数=原子序数,而碳元素为6号元素,故碳元素的核电荷数为6;元素是具有相同质子数的同一类原子的总称,故不同元素的本质区别是质子数不同.故答案为:氧;8;6;质子数不同.
点评 本题考查了微粒种类的判断以及核电荷数和原子序数的关系等问题,难度不大,注意基础的掌握和元素的概念.

练习册系列答案
相关题目
11.下列选项中所涉及到的两个量一定不相等的是( )
| A. | 足量的钠在等物质的量的Cl2和O2中分别燃烧转移电子数 | |
| B. | 等物质的量的KO2与CaO2分别与水反应生成O2的体积(相同条件下) | |
| C. | 100mL 1mol/L HNO3分别与1.4g Fe、2.8gFe完全反应时生成 的NO物质的量 | |
| D. | 等浓度等体积的盐酸、NaOH溶液分别与一定量Al反应生成等质量气体时转移的电子数 |
12.将一定质量的苯完全燃烧,放出的热量为Q,生成的CO2恰好被500mL,1mol/L NaOH溶液吸收生成酸式盐,则同样条件下完全燃烧1mol苯放出的热量是( )
| A. | 12Q | B. | 10Q | C. | 8Q | D. | 6Q |
9.已知26%氨水的密度约为0.91g•cm-3,6%氨水的密度约为0.98g•cm-3若将上述两溶液等体积混合,所得氨水溶液的质量分数是( )
| A. | 等于16% | B. | 大于16% | C. | 小于16% | D. | 无法估算 |
16.将一定质量的甲烷和一氧化碳的混合气体在足量的氧气中充分燃烧,将生成物依次通入盛有足量浓硫酸和氢氧化钠溶液的洗气瓶,实验测得装有浓硫酸的洗气瓶增重5.4克,装有氢氧化钠溶液的洗气瓶增重8.8克.混合气体中甲烷和一氧化碳的物质的量之比为( )
| A. | 12:7 | B. | 3:1 | C. | 1:3 | D. | 1:1 |
6.下列化学用语表述不正确的是( )
| A. | 乙炔分子的结构简式:C2H2 | B. | CH4的球棍模型: | ||
| C. | S2-的结构示意图: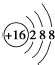 | D. | 乙烯的结构简式:CH2=CH2 |
13.“绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物.下列化学反应符合“绿色化学”理念的是( )
| A. | 制CuSO4:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O | |
| B. | 制CuSO4:CuO+H2SO4(稀)=CuSO4+H2O | |
| C. | 制Cu(NO3)2:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O | |
| D. | 制Cu(NO3)2:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O |
10.下列过程的△H<0的是( )
| A. | Ba(OH)2•8H2O晶体和NH4Cl晶体混合反应 | |
| B. | 煅烧石灰石 | |
| C. | CH3COOH?CH3COO-+H+ | |
| D. | 生石灰溶于水 |
11.下列哪种气体不由两种单质直接化合而成( )
| A. | CO2 | B. | SO2 | C. | NO2 | D. | NO |