题目内容
16.将一定质量的甲烷和一氧化碳的混合气体在足量的氧气中充分燃烧,将生成物依次通入盛有足量浓硫酸和氢氧化钠溶液的洗气瓶,实验测得装有浓硫酸的洗气瓶增重5.4克,装有氢氧化钠溶液的洗气瓶增重8.8克.混合气体中甲烷和一氧化碳的物质的量之比为( )| A. | 12:7 | B. | 3:1 | C. | 1:3 | D. | 1:1 |
分析 CH4和CO组成的混合气体在O2中充分燃烧生成二氧化碳与水,浓硫酸吸水,故浓H2SO4增重5.4克为生成的水的质量,NaOH溶液吸收二氧化碳,所以NaOH溶液增重8.8克为二氧化碳质量,结合水的质量根据氢原子守恒计算甲烷的质量,结合二氧化碳的质量根据碳原子守恒计算一氧化碳的质量,据此进行判断.
解答 解:CH4和CO组成的混合气体在O2中充分燃烧:CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O,2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2,生成二氧化碳与水,
浓硫酸吸水,故浓H2SO4增重5.4克为生成的水的质量,所以生成的水中氢元素的质量为:5.4g×$\frac{2}{18}$=0.6g,
NaOH溶液吸收二氧化碳,故NaOH溶液增重8.8克为二氧化碳质量,所以生成二氧化碳中碳元素的质量:8.8g×$\frac{12}{44}$=2.4g,
根据氢原子守恒,所以甲烷的质量:0.6g÷$\frac{4}{16}$=2.4g,
根据碳原子守恒,一氧化碳中碳元素的质量=二氧化碳中碳元素的质量-甲烷中碳元素的质量=2.4g-(2.4g-0.6g)=0.6g,
所以一氧化碳的质量═0.6g÷$\frac{12}{28}$=1.4g.
所以原混合物中CH4与CO的质量之比为2.4g:1.4g=12:7.
故选A.
点评 本题考查混合物的计算,关键利用原子守恒计算混合物中甲烷与一氧化碳的质量,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列实验能达到目的是( )
| A. | 用湿润的蓝色石蕊试纸检验氨气 | |
| B. | 某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+ | |
| C. | NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 | |
| D. | 将混有HCl的Cl2通入饱和NaHCO3溶液中除去HCl |
11.如表实验中根据现象所得结论正确的是( )
| 操作 | 现象 | 结论 | |
| A | 向某未知溶液中加入盐酸酸化的BaCl2溶液 | 生成白色沉淀 | 该溶液中一定含有SO42- |
| B | 用一束强光照射Na2SiO3溶液 | 溶液中出现一条光亮的通路 | 溶液中可能含有硅酸胶体 |
| C | 向盛有Fe(NO3)2溶液的试管中滴入几滴0.1mol/LH2SO4溶液 | 试管口出现红棕色气体 | 溶液中NO3-被Fe2+还原为NO2 |
| D | 淀粉溶液中加稀硫酸,加热片刻后再滴加银氨溶液,并用水浴加热 | 无银镜生成 | 淀粉未发生水解 |
| A. | A | B. | B | C. | C | D. | D |
5.含碘食盐中加的碘一般是碘酸钾,下列说法正确的是( )
| A. | 碘酸钾易挥发 | |
| B. | 碘酸钾是盐 | |
| C. | 用淀粉就能直接检验碘盐中的碘酸钾 | |
| D. | 碘酸钾可氧化氯化钠 |
6.下列说法正确的是( )
| A. | 淀粉、蛋白质和油脂都是高聚物,在一定条件下都能水解 | |
| B. | 在有机物分子中,含有的氢原子个数一定是偶数 | |
| C. | 乙烯能使酸性高锰酸钾溶液和溴水褪色,二者反应原理相同 | |
| D. | 用溴水可以鉴别己烯、己烷、四氯化碳三种有机物 |
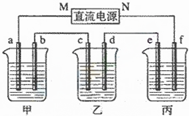 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.85%的NaCl溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.85%的NaCl溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.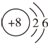 ,该微粒是元素周期表中的氧元素,它的核电荷数是8,碳元素的核电荷数是6,由此可知不同元素的本质区别是质子数不同.
,该微粒是元素周期表中的氧元素,它的核电荷数是8,碳元素的核电荷数是6,由此可知不同元素的本质区别是质子数不同. ,反应类型取代反应.
,反应类型取代反应.