题目内容
在100mL质量分数为36.5%、密度为1.19g/mL的浓盐酸中,加入10.6g Na2CO3粉末,充分搅拌,反应后向溶液中加入足量的AgN03溶液,充分作用.试计算:
(1)该浓盐酸中所含氯离子的物质的量;
(2)不考虑气体的溶解,标准状况下,能放出气体的体积;
(3)加入足量的AgN03溶液后,能生成多少克沉淀(保留三位小数).
(1)该浓盐酸中所含氯离子的物质的量;
(2)不考虑气体的溶解,标准状况下,能放出气体的体积;
(3)加入足量的AgN03溶液后,能生成多少克沉淀(保留三位小数).
考点:化学方程式的有关计算
专题:
分析:(1)根据c=
可知,c(HCl)=
mol/L=11.9mol/L,溶液中氯离子浓度等于HCl的浓度,根据n=cV计算氯离子物质的量;
(2)发生反应:Na2CO3+2HCl=2NaCl+CO2↑+H2O,n(HCl)=11.9mol/L×0.1L=1.19mol,n(Na2CO3)=
=0.1mol,完全反应需要HCl为0.2mol,小于1.19mol,故碳酸钠完全反应,根据碳元素守恒计算二氧化碳物质的量,再根据V=nVm计算二氧化碳体积;
(3)根据氯离子守恒计算n(AgCl),再根据m=nM计算m(AgCl).
| 1000ρω |
| M |
| 1000×1.19×36.5% |
| 36.5 |
(2)发生反应:Na2CO3+2HCl=2NaCl+CO2↑+H2O,n(HCl)=11.9mol/L×0.1L=1.19mol,n(Na2CO3)=
| 10.6g |
| 106g/mol |
(3)根据氯离子守恒计算n(AgCl),再根据m=nM计算m(AgCl).
解答:
解:(1)根据c=
可知,c(HCl)=
mol/L=11.9mol/L,溶液中氯离子浓度等于HCl的浓度,氯离子物质的量为11.9mol/L×0.1L=1.19mol,
答:该浓盐酸中氯离子物质的量为1.19mol;
(2)发生反应:Na2CO3+2HCl=2NaCl+CO2↑+H2O,n(HCl)=11.9mol/L×0.1L=1.19mol,n(Na2CO3)=
=0.1mol,完全反应需要HCl为0.2mol,小于1.19mol,故碳酸钠完全反应,则n(CO2)=n(Na2CO3)=0.1mol,故V(CO2)=0.1mol×22.4L/mol=2.24L,
答:标况下生成二氧化碳的体积为2.24L;
(3)根据氯离子守恒:n(AgCl)=n(Cl-)=1.19mol,则m(AgCl)=1.19mol×143.5g/mol=170.765g,
答:生成沉淀的质量为170.765g.
| 1000ρω |
| M |
| 1000×1.19×36.5% |
| 36.5 |
答:该浓盐酸中氯离子物质的量为1.19mol;
(2)发生反应:Na2CO3+2HCl=2NaCl+CO2↑+H2O,n(HCl)=11.9mol/L×0.1L=1.19mol,n(Na2CO3)=
| 10.6g |
| 106g/mol |
答:标况下生成二氧化碳的体积为2.24L;
(3)根据氯离子守恒:n(AgCl)=n(Cl-)=1.19mol,则m(AgCl)=1.19mol×143.5g/mol=170.765g,
答:生成沉淀的质量为170.765g.
点评:本题考查化学方程式的有关计算,关键是进行过量计算判断HCl有剩余,(3)中注意利用守恒法计算,难度中等.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
某同学不慎受凉感冒发热,他应该服用下面那种药来治疗( )
| A、阿司匹林 | B、青霉素 |
| C、麻黄碱 | D、维生素C |
将锌棒和铁棒按图示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )

| A、将电能转变为化学能 |
| B、电子由铁棒流出 |
| C、锌为正极 |
| D、电池反应为:Zn+CuSO4=ZnSO4+Cu |
下列事实或因果关系正确的是( )
| A、SO2的水溶液能导电说明SO2是电解质 |
| B、某溶液加NaOH溶液加热,产生气体使湿润红色石蕊试纸变蓝,则该溶液含有NH4+ |
| C、HClO是弱酸,所以NaClO是弱电解质 |
| D、某溶液中加入盐酸能产生使澄清石灰水变浑浊气体,则该溶液一定存在大量CO32- |
Na2S、Na2SO3、Na2SO4的混合物,经测定其中含硫的质量分数为25.6%,则混合物中含氧的质量分数为( )
| A、36.8% | B、37.6% |
| C、51.2% | D、无法计算 |
有关化学用语的表示正确的是( )
A、甲烷分子的比例模型是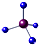 |
B、二氧化碳的电子式: |
C、Cl-的结构示意图为: |
| D、HClO的结构式为H-O-Cl |
根据原子结构及元素周期律的知识,下列推断正确的是( )
| A、Cl?、S2?、Ca2+、K+半径逐渐减小 | ||||
B、
| ||||
| C、同主族元素含氧酸的酸性随核电荷数的增加而减弱 | ||||
| D、核外电子排布相同的微粒化学性质也相同 |
在强酸性溶液中能大量共存的无色透明离子组是( )
| A、K+、Na+、NO3-、CO32- |
| B、Mg2+、Na+、Cl-、SO42- |
| C、K+、Na+、Br-、Cu2+ |
| D、Na+、Ba2+、NO3-、HCO3- |