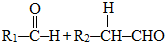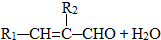题目内容
按下面的实验过程填空:
浅绿色FeBr2溶液
黄色液体

写出上述反应的化学方程式: .
浅绿色FeBr2溶液
| 通足量的Cl2 |
| 1 |
| 加CCl4 |
| 分层 |

写出上述反应的化学方程式:
考点:常见金属元素的单质及其化合物的综合应用
专题:元素及其化合物
分析:FeBr2溶液,通入足量氯气,反应生成FeCl3、Br2,加四氯化碳萃取后,溴溶解在四氯化碳中,且分层后在下层,而上层为氯化铁溶液,氯化铁与KI发生氧化还原反应生成碘,淀粉遇碘变蓝,以此来解答.
解答:
解:FeBr2溶液,通入足量氯气,反应生成FeCl3、Br2,加四氯化碳萃取后,溴溶解在四氯化碳中,且分层后在下层,而上层为氯化铁溶液,氯化铁与KI发生氧化还原反应生成碘,淀粉遇碘变蓝,由上述分析可知,上层a(氯化铁溶液)为棕黄色,下层b(溴的四氯化碳溶液)为橙红色,c为蓝色,上述反应的化学方程式为2FeBr2+3Cl2═2FeCl3+2Br2、2FeCl3+2KI═2FeCl2+2KCl+I2,
故答案为:棕黄;橙红;蓝;2FeBr2+3Cl2═2FeCl3+2Br2、2FeCl3+2KI═2FeCl2+2KCl+I2.
故答案为:棕黄;橙红;蓝;2FeBr2+3Cl2═2FeCl3+2Br2、2FeCl3+2KI═2FeCl2+2KCl+I2.
点评:本题考查常见金属铁及其化合物的性质,为高频考点,把握发生的氧化还原反应、萃取及现象等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
200℃时,11.6g CO2和水蒸气的混合气体与足量的Na2O2充分反应后,固体质量增加了3.6g,则原混合气体的平均摩尔质量为( )
| A、5.8 g?mol-1 |
| B、11.6 g?mol-1 |
| C、23.2 g?mol-1 |
| D、46.4 g?mol-1 |
短周期元素R、T、X、Y、Z在元素周期表的相对位置如表所示,它们的核外电子数之和为58.则下列判断不正确的是( )
| R | T | |
| X | Y | Z |
| A、R的其中一种单质可用做电极材料 |
| B、五种元素中原子半径最大的是X |
| C、气态氢化物稳定性:Y>T |
| D、Z元素的最高价氧化物对应的水化物的化学式为HZO4 |
某碱性无色溶液中加入BaCl2溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解,则该溶液中存在的离子可能为( )
| A、Ag+ |
| B、SO42- |
| C、CO32- |
| D、Cu2+ |
某未知溶液可能含Cl-、CO32-、Na+、SO42-、Al3+,将溶液滴在蓝色石蕊试纸上,试纸变红.取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀.下列判断合理的是①一定有Cl-,②一定有SO42-,③一定没有Al3+,④一定没有CO32-.( )
| A、①② | B、③④ | C、①③ | D、②④ |
下列关于油脂的叙述不正确的是( )
| A、油脂是一种混合物 |
| B、油脂属于酯类 |
| C、油脂是高级脂肪酸甘油酯 |
| D、油脂都不能使溴水褪色 |
已知某镍镉(Ni-Cd)电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O
Cd(OH)2+2Ni(OH)2.有关该电池的说法正确的是( )
| 放电 |
| 充电 |
| A、充电时阳极的反应式为:Ni(OH)2-e-+OH-=NiOOH+H2O |
| B、充电时将镍镉电池的正极与外加直流电源的负极相连 |
| C、放电时负极附近溶液的碱性不变 |
| D、放电时电解质溶液中的OH-向正极移动 |
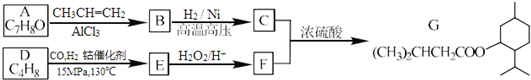
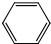 +CH2=CH2
+CH2=CH2