题目内容
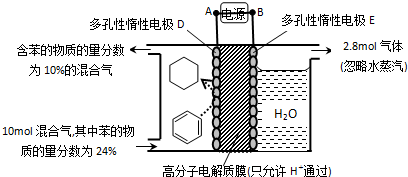
 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热某废塑料得到的产物如表:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热某废塑料得到的产物如表:| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
物与氢气加成后所得产物的一氯代物有
(2)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔.A中残留物
| ① |
| ② |
| ③ |
写出反应②的化学方程式
(3)ZnC2、Al4C3、Mg2C3、Li2C2、Mg3N2等与CaC2和H2O反应相似.请通过对CaC2制C2H2的反应的思考,判断下列反应产物正确的是
A.ZnC2水解生成乙烷(C2H6) B.Al4C3水解生成甲烷(CH4)
C.Mg2C3水解生成丙炔(C3H4) D.Li2C2水解生成乙烯(C2H4)
E.Mg3N2水解生成氨气(NH3)
考点:塑料的老化和降解
专题:有机化合物的获得与应用
分析:(1)核磁共振氢谱有几个峰就有几种等效氢原子;
(2)碳化钙和水反应制取乙炔同时生成氢氧化钙;
(3)ZnC2、Al4C3、Mg2C3、Li2C2、Mg3N2等同属于离子型碳化物,已知CaC2+2H2O→C2H2↑+Ca(OH)2,根据原子守恒分别写出离子型碳化物与水反应的方程式,在判断选项中产物是否正确.
(2)碳化钙和水反应制取乙炔同时生成氢氧化钙;
(3)ZnC2、Al4C3、Mg2C3、Li2C2、Mg3N2等同属于离子型碳化物,已知CaC2+2H2O→C2H2↑+Ca(OH)2,根据原子守恒分别写出离子型碳化物与水反应的方程式,在判断选项中产物是否正确.
解答:
解:(1)核磁共振氢谱显示有四个吸收峰,说明有4个等效氢原子,常温下为液体,只有甲苯符合,与氢气加成后所得产物为甲基环己烷,一氯代物有5种,故答案为:5;
(2)反应②是碳化钙与水反应,反应的化学方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑,故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
(3)A.ZnC2与水反应生成Zn(OH)2,根据原子守恒得:ZnC2+2H2O→Zn(OH)2+C2H2↑,所以另一种产物为C2H2,故A错误;
B.Al4C3与水反应生成Al(OH)3,根据原子守恒得:Al4C3+12H2O→4Al(OH)3+3CH4↑,所以所以另一种产物为CH4,故B正确;
C.Mg2C3与水反应生成Mg(OH)2,根据原子守恒得:Mg2C3+4H2O→2Mg(OH)2+C3H4↑,所以另一种产物为C3H4,故C正确;
D.Li2C2与水反应生成Zn(OH)2,根据原子守恒得:Li2C2+2H2O→2LiOH+C2H2↑,所以另一种产物为C2H2,故D错误;
E.Mg3N2与水反应生成Mg(OH)2,根据原子守恒得:Mg3N2+6H2O→3Mg(OH)2+2NH3↑,所以另一种产物为NH3,故E正确.
故答案为:BCE.
(2)反应②是碳化钙与水反应,反应的化学方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑,故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
(3)A.ZnC2与水反应生成Zn(OH)2,根据原子守恒得:ZnC2+2H2O→Zn(OH)2+C2H2↑,所以另一种产物为C2H2,故A错误;
B.Al4C3与水反应生成Al(OH)3,根据原子守恒得:Al4C3+12H2O→4Al(OH)3+3CH4↑,所以所以另一种产物为CH4,故B正确;
C.Mg2C3与水反应生成Mg(OH)2,根据原子守恒得:Mg2C3+4H2O→2Mg(OH)2+C3H4↑,所以另一种产物为C3H4,故C正确;
D.Li2C2与水反应生成Zn(OH)2,根据原子守恒得:Li2C2+2H2O→2LiOH+C2H2↑,所以另一种产物为C2H2,故D错误;
E.Mg3N2与水反应生成Mg(OH)2,根据原子守恒得:Mg3N2+6H2O→3Mg(OH)2+2NH3↑,所以另一种产物为NH3,故E正确.
故答案为:BCE.
点评:本题考查有机物的结构、离子型碳化物的水解反应,注意类比迁移思想的应用和原子守恒的应用,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如图所示,利用海水可提取很多重要的化工原料,下列有关说法不正确的是.( ) 

| A、第②步是MgCl2?6H2O在坩埚中加强热分解 |
| B、第①步是海水蒸发浓缩、结晶过滤 |
| C、第③、⑤步可以是通入足量Cl2 |
| D、在第④步反应为:Br2+SO2+2H2O=H2SO4+2HBr |
下列各操作中,正确的是( )
| A、为减缓反应速率,用饱和食盐水与电石反应制乙炔 |
| B、进行酸碱中和滴定时,锥形瓶应用待测液润洗 |
| C、实验室制乙烯时应将无水乙醇缓慢加入浓硫酸中,并加入碎瓷片以防爆沸 |
| D、配制FeCl3溶液时,向试管中加入少量Fe和稀盐酸 |
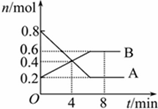 某温度时,在0.5L密闭容器中某一反应的A,B气体物质随时间变化的曲线如图所示,由图中数据分析求得:
某温度时,在0.5L密闭容器中某一反应的A,B气体物质随时间变化的曲线如图所示,由图中数据分析求得: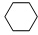 (g)
(g)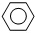 (g)+3H2(g)
(g)+3H2(g)