题目内容
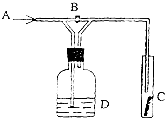 如图是一种试验某种气体化学性质的实验装置,图中B为开关.如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去.则D瓶盛的溶液是( )
如图是一种试验某种气体化学性质的实验装置,图中B为开关.如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去.则D瓶盛的溶液是( )| A、浓硫酸 |
| B、饱和食盐水 |
| C、浓氢氧化钠溶液 |
| D、氢氧化钙悬浊液 |
考点:探究氯水、氯气的漂白作用
专题:卤族元素
分析:干燥氯气不能使有色布条褪色,当关闭B时,气体经过D装置,C处红色布条颜色褪去,说明氯气通过D装置后,含有水蒸气.
解答:
解:A.氯气经过盛有浓硫酸的洗气瓶,为干燥氯气,不能使有色布条褪色,故A错误;
B.氯气难溶于饱和食盐水,经过饱和食盐水后,氯气中混有水,能生成具有漂白性的HClO,可使有色布条褪色,故B正确;
C.氯气经过盛有NaOH溶液的洗气瓶而被吸收,则有色布条不褪色,故C错误;
D、氯气经氢氧化钙后,氯气被吸收,则有色布条不褪色,故D错误;
故选B.
B.氯气难溶于饱和食盐水,经过饱和食盐水后,氯气中混有水,能生成具有漂白性的HClO,可使有色布条褪色,故B正确;
C.氯气经过盛有NaOH溶液的洗气瓶而被吸收,则有色布条不褪色,故C错误;
D、氯气经氢氧化钙后,氯气被吸收,则有色布条不褪色,故D错误;
故选B.
点评:本题考查氯气的性质,题目难度不大,本题注意氯气使有色布条褪色的原因是能生成具有漂白性的HClO.

练习册系列答案
相关题目
已知CH4、H2O和NH3的物质的量均为1mol,下列说法不正确的是( )
| A、所含分子数之比为1:1:1 |
| B、所含氢原子数之比为4:2:3 |
| C、摩尔质量之比为1:1:1 |
| D、质量之比为16:18:17 |
在一定温度下,反应A2(气)+B2(气)?2AB(气)达到平衡的标志是( )
| A、单位时间生成n mol的A2同时生成n mol的AB |
| B、容器内的总压强不随时间变化 |
| C、单位时间生成2n mol的AB同时生成n mol的B2 |
| D、单位时间生成n mol的A2同时生成n mol的B2 |
以下说法:①SO2、SiO2、CO均为酸性氧化物
②KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质
③碱性氧化物一定是金属氧化物
④硫酸、火碱、纯碱、生石灰分别属于酸、碱、盐和氧化物
⑤二氧化硅的分子式为SiO2,酸性氧化物,能与NaOH溶液反应
⑥正四面体分子中键角一定是109°28′
⑦CO2 与SiO2化学性质相似物理性质也相似
⑧福尔马林、水玻璃、氨水均为混合物
⑨强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
其中正确的是( )
②KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质
③碱性氧化物一定是金属氧化物
④硫酸、火碱、纯碱、生石灰分别属于酸、碱、盐和氧化物
⑤二氧化硅的分子式为SiO2,酸性氧化物,能与NaOH溶液反应
⑥正四面体分子中键角一定是109°28′
⑦CO2 与SiO2化学性质相似物理性质也相似
⑧福尔马林、水玻璃、氨水均为混合物
⑨强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
其中正确的是( )
| A、①③④⑤⑥ | B、④⑥⑧⑨ |
| C、③④⑧ | D、②④⑦⑨ |
下列物质间的转化在给定条件下能够实现的是( )
①Al2O3
NaAlO2(aq)或Na[Al(OH)4](aq)
Al(OH)3
②S
SO3
H2SO4
③NaOH(aq)
NaHCO3
Na2CO3
④Fe2O3
FeCl3(aq)
无水FeCl3
⑤NH4Cl(s)
NH3
NH4HCO3.
①Al2O3
| NaOH(aq) |
| △ |
| CO2 |
②S
| O2 |
| 点燃 |
| H2O |
③NaOH(aq)
| 足量CO2 |
| △ |
④Fe2O3
| HCl(aq) |
| △ |
⑤NH4Cl(s)
| 熟石灰 |
| △ |
| H2O、CO2 |
| A、①③⑤ | B、②③④ |
| C、②④⑤ | D、①④⑤ |
化学与生产、生活、社会密切相关.下列有关说法中,错误的是( )
| A、服用铬含量超标的药用胶囊会对人体健康造成危害 |
| B、镀层破坏后,镀锡铁板比镀锌铁板更耐腐蚀 |
| C、关闭高能耗的化工企业,体现了“低碳经济”的宗旨 |
| D、雾霾主要是由化石燃料燃烧排放的二氧化硫、氮氧化物、烟尘以及机动车尾气、建筑扬尘等导致的 |
