题目内容
下列物质间的转化在给定条件下能够实现的是( )
①Al2O3
NaAlO2(aq)或Na[Al(OH)4](aq)
Al(OH)3
②S
SO3
H2SO4
③NaOH(aq)
NaHCO3
Na2CO3
④Fe2O3
FeCl3(aq)
无水FeCl3
⑤NH4Cl(s)
NH3
NH4HCO3.
①Al2O3
| NaOH(aq) |
| △ |
| CO2 |
②S
| O2 |
| 点燃 |
| H2O |
③NaOH(aq)
| 足量CO2 |
| △ |
④Fe2O3
| HCl(aq) |
| △ |
⑤NH4Cl(s)
| 熟石灰 |
| △ |
| H2O、CO2 |
| A、①③⑤ | B、②③④ |
| C、②④⑤ | D、①④⑤ |
考点:镁、铝的重要化合物,铵盐,含硫物质的性质及综合应用,钠的重要化合物,铁的氧化物和氢氧化物
专题:元素及其化合物
分析:①氧化铝与氢氧化钠反应生成偏铝酸钠,偏铝酸钠溶液通入二氧化碳,生成氢氧化铝.
②硫燃烧生成二氧化硫.
③在氢氧化钠溶液中通入过量的二氧化碳,生成碳酸氢钠,加热NaHCO3分解生成碳酸钠.
④三氧化二铁与盐酸反应生成氯化铁溶液,因为三价铁水解生成易挥发的氯化氢气体,所以加热得到氢氧化铁;
⑤NH4Cl与熟石灰反应生成氨气,通入二氧化碳和水反应生成碳酸氢铵.
②硫燃烧生成二氧化硫.
③在氢氧化钠溶液中通入过量的二氧化碳,生成碳酸氢钠,加热NaHCO3分解生成碳酸钠.
④三氧化二铁与盐酸反应生成氯化铁溶液,因为三价铁水解生成易挥发的氯化氢气体,所以加热得到氢氧化铁;
⑤NH4Cl与熟石灰反应生成氨气,通入二氧化碳和水反应生成碳酸氢铵.
解答:
解:①氧化铝与氢氧化钠反应生成偏铝酸钠,偏铝酸钠溶液通入二氧化碳,发生反应2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO3,生成氢氧化铝,故①正确;
②硫燃烧生成二氧化硫,不能生成三氧化硫,故②错误;
③在氢氧化钠溶液中通入过量的二氧化碳,生成碳酸氢钠,加热NaHCO3分解生成碳酸钠,故③正确;
④三氧化二铁与盐酸反应生成氯化铁溶液,因为三价铁水解生成易挥发的氯化氢气体,所以加热得到氢氧化铁,故④错误;
⑤NH4Cl与熟石灰反应生成氨气,通入二氧化碳和水反应生成碳酸氢铵,故⑤正确.
故选:A.
②硫燃烧生成二氧化硫,不能生成三氧化硫,故②错误;
③在氢氧化钠溶液中通入过量的二氧化碳,生成碳酸氢钠,加热NaHCO3分解生成碳酸钠,故③正确;
④三氧化二铁与盐酸反应生成氯化铁溶液,因为三价铁水解生成易挥发的氯化氢气体,所以加热得到氢氧化铁,故④错误;
⑤NH4Cl与熟石灰反应生成氨气,通入二氧化碳和水反应生成碳酸氢铵,故⑤正确.
故选:A.
点评:考查元素化合性质、侯德榜制碱法,难度中等,注意侯德榜制碱法要先通氨气,后通二氧化碳,以便获得高浓度离子溶液.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列结论正确的是( )
| A、向氯化铝溶液中滴加过量氨水,反应的离子方程式是:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、足量铜与含1mol溶质的浓硫酸反应,可生成0.5molSO2 |
| C、溶液与胶体:本质不同的原因是能否发生丁达尔效应 |
| D、15.6g过氧化钠与足量二氧化碳充分反应,转移电子数为1.204×1023 |
在核反应方程
He+
N→
O+X中,X代表的粒子是( )
4 2 |
14 7 |
17 8 |
A、
| ||
B、
| ||
C、
| ||
D、
|
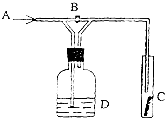 如图是一种试验某种气体化学性质的实验装置,图中B为开关.如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去.则D瓶盛的溶液是( )
如图是一种试验某种气体化学性质的实验装置,图中B为开关.如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去.则D瓶盛的溶液是( )| A、浓硫酸 |
| B、饱和食盐水 |
| C、浓氢氧化钠溶液 |
| D、氢氧化钙悬浊液 |
X、Y、Z为三种气体,把amolX和bmolY充入一密闭容器中,发生反应X+2Y?2Z.达到平衡时,若他们的物质的量满足:n(X)+n(Y)=n(Z)则Y的转化率为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
用四氯化碳萃取碘水中的碘,下列说法中不正确的是( )
| A、实验使用的主要仪器是分液漏斗 |
| B、碘在四氯化碳中的溶解度比在水中的溶解度大 |
| C、碘的四氯化碳溶液呈紫红色 |
| D、分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出 |
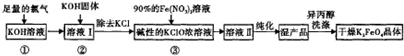
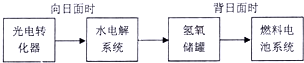
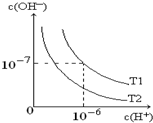 如图是在温度T1、T2时溶液中c(H+)、c(OH-)变化关系图,试回答:
如图是在温度T1、T2时溶液中c(H+)、c(OH-)变化关系图,试回答: