题目内容
2.下列表达方式错误的是( )| A. | 氟化钠的电子式为  | B. | 氯原子的结构示意图: | ||
| C. | CO2分子的结构式:O=C=O | D. | 甲烷的电子式  |
分析 A.氟化钠是离子化合物,由氟离子与钠离子构成;
B.氯原子是17号元素分为三个电子层,一层2个电子,二层8个电子.三层7个电子,图中小圈表示氯的原子核,圈内数字表示 质子数,弧线表示电子层,弧线上面的数字表示该层的电子数;
C.二氧化碳是直线形结构,每个氧原子和碳原子形成碳氧双键;
D.甲烷分子中碳原子最外层有4个电子,能形成4个共价键达到稳定结构,每个氢原子能形成一个共价键达到稳定结构,据此写出甲烷的电子式.
解答 解:A.氟化钠是离子化合物,由氟离子与钠离子构成,氟化钠的电子式: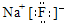 ,故A正确;
,故A正确;
B.氯原子是17号元素,核外电子分为三个电子层,一层2个电子,二层8个电子.三层7个电子,原子结构示意图为 ,选项中是离子结构示意图,故B错误;
,选项中是离子结构示意图,故B错误;
C.二氧化碳是直线形结构,每个氧原子和碳原子形成碳氧双键,其结构式为O=C=O,故C正确;
D.因碳原子的最外层有4个电子,氢原子最外层1个电子,一个碳原子形成4对共用电子对,一个氢原子形成一对共用电子对,所以电子式为 ,
,
故D正确;
故选B.
点评 本题考查电子式、元素、球棍模型和水解方程式的书写,题目难度不大,注意电子式书写方法和离子化合物、共价化合物的书写方法.

练习册系列答案
相关题目
13.己知钡的活动性处于Na、K之间,则下列说法中可能实现的是( )
| A. | Ba可从KCl溶液中置换出钾 | |
| B. | Ba 可从冷水中置换出氢 | |
| C. | 在溶液中Zn可还原Ba2+生成Ba | |
| D. | Ba投入到NaOH溶液中,没有明显的现象 |
14.化学与生活密切相关,下列说法正确的是( )
| A. | 汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的 | |
| B. | 日常生活中,卤水点豆腐、花生中提取花生油、海水晒盐都是物理变化 | |
| C. | 食品保鲜膜、塑料水杯等生活用品的主要成分是聚氯乙烯 | |
| D. | 铝比铁活泼,所以一般情况下,铁制品比铝制品更耐腐蚀 |
10.为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格.
供选择的化学试剂及实验方法:
A、酸性高锰酸钾,观察现象 B、滴加酚酞试液,观察现象
C、用淀粉碘化钾试纸,观察现象 D、加入NaOH浓溶液加热,观察现象.
| 实 验 目 的 | 试剂及方法 |
| 证明NaOH溶液具有碱性 | B |
| 鉴别Na2SO4溶液和(NH4)2SO4溶液 | D |
| 检验自来水中是否含有Cl2 | C |
| 区别CH4和C2H4两种无色气体 | A |
A、酸性高锰酸钾,观察现象 B、滴加酚酞试液,观察现象
C、用淀粉碘化钾试纸,观察现象 D、加入NaOH浓溶液加热,观察现象.
17.不符合工业治炼金属情况的是( )
| A. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ | B. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | ||
| C. | 2MgO$\frac{\underline{\;\;△\;\;}}{\;}$2Mg+O2↑ | D. | MgCl2$\frac{\underline{\;电解\;}}{熔融}$Mg+Cl2↑ |
7.将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).下列可以判断该分解反应已经达到化学平衡状态的是( )
| A. | v(NH3)=2v(CO2) | |
| B. | 密闭容器中混合气体的平均摩尔质量不变 | |
| C. | 密闭容器中混合气体密度不变 | |
| D. | 密闭容器中氨气的体积分数不变 |
14.下列说法正确的是( )
| A. | 氢氧燃料电池工作时,H2在负极上失去电子 | |
| B. | 0.1mol/LNa2CO3溶液加热后,溶液的PH减小 | |
| C. | 中和滴定时,滴定管用所盛装的反应液润洗2〜3次 | |
| D. | 室温下,稀释0.1mol/LCH3COOH溶液,溶液的导电能力增强 |
11.下列装置或操作能达到实验目的是( )
| A. |  验证铁的吸氧腐蚀 | B. |  测定双氧水分解速率 | ||
| C. |  蒸干MgCl2溶液制备MgCl2固体 | D. |  模拟合成氨并验证有氨气生成 |
12.下列有关说法正确的是( )
| A. | 活化分子之间发生的碰撞一定为有效碰撞 | |
| B. | 升高温度,降低反应的活化能,可使活化分子的百分数增大,因而反应速率增大 | |
| C. | 金属腐蚀就是金属失去电子被氧化的过程 | |
| D. | 电解法精炼铜时,以粗铜作阳极,粗铜中的所有金属都以离子的形式进入电解质溶液 |