题目内容
下列离子方程式正确的是( )
| A、用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑ | ||
B、苯酚与碳酸钠反应:2C6H5OH+C
| ||
| C、苯酚钠溶液中通入少量CO2:CO2+H2O+C6H5O -→C6H5OH+HCO3- | ||
| D、乙酸乙酯与氢氧化钠溶液反应:CH3COOC2H5+OH-→CH3COOH+C2H5O - |
考点:离子方程式的书写
专题:离子反应专题
分析:A、醋酸为弱酸,应写成化学式,碳酸钙不溶于水,离子方程式中应写成化学式;
B、苯酚的酸性比碳酸的酸性弱,不符合客观事实;
C、苯酚为弱酸,应写成化学式,强制弱;
D、乙醇是非电解质,应写成化学式.
B、苯酚的酸性比碳酸的酸性弱,不符合客观事实;
C、苯酚为弱酸,应写成化学式,强制弱;
D、乙醇是非电解质,应写成化学式.
解答:
解:A、醋酸为弱酸,应写成化学式,碳酸钙不溶于水,离子方程式中应写成化学式,正确的离子方程式为CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O,故A错误;
B、苯酚的酸性比碳酸的酸性弱,不符合客观事实,正确的离子方程式为C6H5OH+CO32-=C6H5O -+HCO3-,故B错误;
C、苯酚为弱酸,应写成化学式,强制弱,离子方程式为CO2+H2O+C6H5O -→C6H5OH+HCO3-,故C正确;
D、乙醇是非电解质,应写成化学式,正确的离子方程式为CH3COOC2H5+OH-→CH3COO-+C2H5OH,故D错误;
故选C.
B、苯酚的酸性比碳酸的酸性弱,不符合客观事实,正确的离子方程式为C6H5OH+CO32-=C6H5O -+HCO3-,故B错误;
C、苯酚为弱酸,应写成化学式,强制弱,离子方程式为CO2+H2O+C6H5O -→C6H5OH+HCO3-,故C正确;
D、乙醇是非电解质,应写成化学式,正确的离子方程式为CH3COOC2H5+OH-→CH3COO-+C2H5OH,故D错误;
故选C.
点评:本题考查离子方程式的书写,题目难度不大,注意从化学式、离子符号、电荷守恒以及是否符合反应实际的角度分析.

练习册系列答案
相关题目
溴化碘(IBr)的化学性质跟Cl2单质相似,它跟水反应的化学方程式为:IBr+H2O=HBr+HIO,下列有关的叙述中,不正确的是( )
| A、IBr是双原子分子 |
| B、在很多反应中,IBr是氧化剂 |
| C、和NaOH溶液反应只生成NaBr |
| D、和H2O反应时,IBr既是不氧化剂又不是还原剂 |
下列各组物质全部是弱电解质的是( )
| A、H2SiO3 H2S CO2 |
| B、MgSO4 CH3COOH CH3CH2OH |
| C、H2SO3 BaSO4 CH4 |
| D、H2O NH3?H2O H3PO4 |
下列说法正确的是( )
| A、胶体不是一种化合物,而是一种混合物 |
| B、电离时生成H+,则该化合物为酸 |
| C、在水溶液和熔化状态下均能导电的化合物叫电解质 |
| D、离子方程式只表示同一类型的离子反应,不表示某一个具体的化学反应 |
下列各组离子中,在pH=1的溶液中能大量共存且为无色透明溶液的是( )
| A、K+、HCO3-、Na+、SO42- |
| B、NH4+、SO42-、Ba2+、Cl- |
| C、Na+、MnO4-、NO3-、K+ |
| D、Na+、SO42-、Mg2+、Cl- |
已知aXm+、bYn+、cXn-、dRm-四种离子的电子层结构相同(a、b、c、d为元素的核电荷数),则下列关系正确的是( )
| A、a-c=m-n |
| B、a-b=n-m |
| C、c-d=m+n |
| D、a-c=n+m |
 化学概念在逻辑上存在如图所示关系:对下列概念的说法不正确的是
化学概念在逻辑上存在如图所示关系:对下列概念的说法不正确的是( )
| A、纯净物与混合物属于并列关系 |
| B、化合物与氧化物属于包含关系 |
| C、单质与化合物属于交叉关系 |
| D、氧化还原反应与化合反应属于交叉关系 |
下列说法不正确的是( )
| A、固体NaCl不导电,但 NaCl是电解质 |
| B、CO2的水溶液导电,但 CO2不是电解质 |
| C、铜、石墨均导电,但它们均不是电解质 |
| D、稀硫酸能导电,所以稀硫酸是电解质 |
下列轨道表示式能表示磷原子的最低能量状态的是( )
A、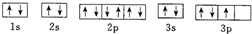 |
B、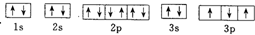 |
C、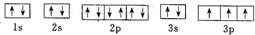 |
D、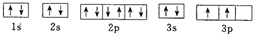 |