题目内容
下列各组物质全部是弱电解质的是( )
| A、H2SiO3 H2S CO2 |
| B、MgSO4 CH3COOH CH3CH2OH |
| C、H2SO3 BaSO4 CH4 |
| D、H2O NH3?H2O H3PO4 |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:强电解质是指:在水溶液中或熔融状态下,能够完全电离的化合物.一般包括强酸、强碱和大部分盐类;
弱电解质是指:在水溶液里部分电离的电解质,包括弱酸、弱碱、水与少数盐.据此即可解答.
弱电解质是指:在水溶液里部分电离的电解质,包括弱酸、弱碱、水与少数盐.据此即可解答.
解答:
解:A.H2SiO3 H2S 在水中能部分电离,属于弱电解质,二氧化碳本身在水中或者熔融状态下不能电离,属于非电解质,故A错误;
B.MgSO4 为盐,在水溶液中或熔融状态下,能够完全电离,为强电解质,CH3COOH在水溶液中能部分电离为弱电解质,CH3CH2OH在水中或者熔融状态下不能电离,属于非电解质,故B错误;
C.BaSO4 熔融状态下,能够完全电离,为强电解质,H2SO3水溶液中能部分电离为弱电解质,CH4在水中或者熔融状态下不能电离,属于非电解质,故C错误;
D.H2O NH3?H2O H3PO4 三种物质在水溶液中部分电离,都属于弱电解质,故D正确;
故选:D.
B.MgSO4 为盐,在水溶液中或熔融状态下,能够完全电离,为强电解质,CH3COOH在水溶液中能部分电离为弱电解质,CH3CH2OH在水中或者熔融状态下不能电离,属于非电解质,故B错误;
C.BaSO4 熔融状态下,能够完全电离,为强电解质,H2SO3水溶液中能部分电离为弱电解质,CH4在水中或者熔融状态下不能电离,属于非电解质,故C错误;
D.H2O NH3?H2O H3PO4 三种物质在水溶液中部分电离,都属于弱电解质,故D正确;
故选:D.
点评:本题主要考查了强、弱电解质的判断,抓住弱电解质的特征“不能完全电离”,注意积累常见的弱电解质有助于解题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在下列实验操作中错误的是( )
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计的水银球放置于蒸馏烧瓶的支管出口稍下处 |
| C、用容量瓶配制溶液时,加水超过了刻度线,没有采取补救措施,重新配制 |
| D、将5.85gNaCl溶于100mL水中,即配成1.0 mol/L NaCl溶液 |
下列反应属于氧化还原反应但不属于置换反应的是( )
| A、NaOH+HCl=NaCl+H2O | ||||
B、C+H2O
| ||||
| C、2Na+2H2O=2NaOH+H2↑ | ||||
| D、2Na2O2+2H2O═4NaOH+O2↑ |
下列关于价电子构型为3s23p4的粒子描述正确的是( )
| A、它的原子核外有三种形状不同的电子云 |
| B、它的原子核外电子共有16种不同的运动状态 |
| C、它可与H2反应生成的化合物为非极性分子 |
D、核外电子轨道表示式为: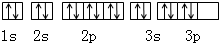 |
下列关于含Na元素、C1元素的物质的性质叙述正确的是( )
| A、Na单质在空气中缓慢氧化与燃烧的产物都是Na2O2 |
| B、Na2O与Na2O2都能与水反应,产物相同 |
| C、C12与H2混合光照爆炸,H2在C12也能平静的燃烧 |
| D、C12能与NaOH溶液反应,S单质与NaOH溶液加热也不反应 |
| E、C12能与NaOH溶液反应,S单质与NaOH溶液加热也不反应 |
下列各组粒子中属于同位素的是( )
| A、24Mg和24Na |
| B、H2O和D2O |
| C、H2和D2 |
| D、16O和18O |
下列离子方程式正确的是( )
| A、用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑ | ||
B、苯酚与碳酸钠反应:2C6H5OH+C
| ||
| C、苯酚钠溶液中通入少量CO2:CO2+H2O+C6H5O -→C6H5OH+HCO3- | ||
| D、乙酸乙酯与氢氧化钠溶液反应:CH3COOC2H5+OH-→CH3COOH+C2H5O - |
在下面的价层电子构型中,第一电离能最小的原子是( )
| A、2s22p3 |
| B、3s23p5 |
| C、3s23p4 |
| D、3s23p6 |