��Ŀ����
��ѧ��һֱ�����ڡ��˹��̵������·����о���
��l��Ŀǰ�ϳɰ�����ԭ��Ϊ��N2��g��+3H2��g��?2NH3��g����H=-92.4KJ/molNH3��������ˮ����ˮ��Һ�׳ư�ˮ����ˮϡ��0.1mol/L�İ�ˮ����Һ������ˮ�������Ӷ���С���� ������ţ���
a.
b.
c��c��H+����c��OH-��d.
��2��1998��ϣ������ʿ��´�ѧ����λ��ѧ�Ҳ��ø����ӵ����Ե�SCYȽ�ɣ��ܴ���H+����ʵ���˸��³�ѹ������N2��H2���ϳɰ����������ĵ缫��Ӧʽ ��
��3���������¡��˹��̵������о��������ڳ��¡���ѹ�����������£�N2�ڴ�������������Fe2O3��TiO2��������ˮ�������з�Ӧ��2N2��g��+6HO��1��?4NH3��g��+3O2��g����H=aKJ/mol��һ���о�NH3���������¶ȵĹ�ϵ����ѹ�´ﵽƽ��ʱ��ò���ʵ���������
�ٴ˺ϳɷ�Ӧ��a 0����S 0�����������������=������
����֪��N2��g��+3H2��g��?2NH3��g����H=-92.4KJ/mol��
2H2��g��+O2��g��=2H2O��g����H=-571.6KJ/mol
��2N2��g��+6H2O��g��=4NH��g��+3O2��g����H= ��
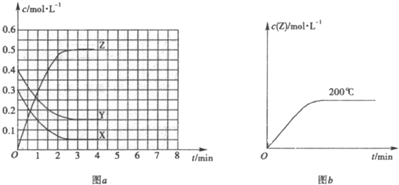
����֪���淴Ӧ��δ��ƽ��X��g��+Y��g��?Z��g����H��0���¶�ΪT0ʱ�����ݻ��̶��������з�����Ӧ�������ʵ�Ũ����ʱ��仯�Ĺ�ϵ��ͼa��ʾ��
��1��T0��ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ
��2��ͼbΪ200��ʱ������c ��Z���ı仯���ߣ�����ͼ�в����÷�Ӧ��100��ʱ��c ��Z���ı仯���ߣ�
��l��Ŀǰ�ϳɰ�����ԭ��Ϊ��N2��g��+3H2��g��?2NH3��g����H=-92.4KJ/molNH3��������ˮ����ˮ��Һ�׳ư�ˮ����ˮϡ��0.1mol/L�İ�ˮ����Һ������ˮ�������Ӷ���С����
a.
c(N
| ||
| c(NH��3H2O) |
| c(NH��3H2O) |
| c(OH-) |
| c(OH-) |
| c(H+) |
��2��1998��ϣ������ʿ��´�ѧ����λ��ѧ�Ҳ��ø����ӵ����Ե�SCYȽ�ɣ��ܴ���H+����ʵ���˸��³�ѹ������N2��H2���ϳɰ����������ĵ缫��Ӧʽ
��3���������¡��˹��̵������о��������ڳ��¡���ѹ�����������£�N2�ڴ�������������Fe2O3��TiO2��������ˮ�������з�Ӧ��2N2��g��+6HO��1��?4NH3��g��+3O2��g����H=aKJ/mol��һ���о�NH3���������¶ȵĹ�ϵ����ѹ�´ﵽƽ��ʱ��ò���ʵ���������
| T/K | 303 | 313 | 323 |
| NH3������/��10-6mol�� | 4.8 | 5.9 | 6.0 |
����֪��N2��g��+3H2��g��?2NH3��g����H=-92.4KJ/mol��
2H2��g��+O2��g��=2H2O��g����H=-571.6KJ/mol
��2N2��g��+6H2O��g��=4NH��g��+3O2��g����H=
����֪���淴Ӧ��δ��ƽ��X��g��+Y��g��?Z��g����H��0���¶�ΪT0ʱ�����ݻ��̶��������з�����Ӧ�������ʵ�Ũ����ʱ��仯�Ĺ�ϵ��ͼa��ʾ��
��1��T0��ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ
��2��ͼbΪ200��ʱ������c ��Z���ı仯���ߣ�����ͼ�в����÷�Ӧ��100��ʱ��c ��Z���ı仯���ߣ�

���㣺��ѧƽ��ļ���,ԭ��غ͵��صĹ���ԭ��,���������ˮ��Һ�еĵ���ƽ��
ר�⣺
��������1����ˮϡ�ͣ��ٽ�һˮ�ϰ��ĵ��룬ƽ�����������ƶ���
��2�����ص����������õ��ӵĻ�ԭ��Ӧ��
��3�����ɱ��������ж������¶�ƽ���ƶ��ķ����Դ��жϷ�Ӧ�ȣ�
�������ʵľۼ�״̬�жϡ�S�������ݸ�˹���ɽ��з������㣬ͨ���ϲ��Ȼ�ѧ����ʽ�õ��ʱ䣻
��1������ͼ������ж�ƽ��״̬��Ӧ���������ƽ��Ũ�ȣ����ƽ�ⳣ��������ʽ���㣻
��2�����ݡ��ȹ���ƽ����ֵ�������¶ȣ�Z�����ʵ���Ũ������ƽ��������Ӧ�����ƶ���
��2�����ص����������õ��ӵĻ�ԭ��Ӧ��
��3�����ɱ��������ж������¶�ƽ���ƶ��ķ����Դ��жϷ�Ӧ�ȣ�
�������ʵľۼ�״̬�жϡ�S�������ݸ�˹���ɽ��з������㣬ͨ���ϲ��Ȼ�ѧ����ʽ�õ��ʱ䣻
��1������ͼ������ж�ƽ��״̬��Ӧ���������ƽ��Ũ�ȣ����ƽ�ⳣ��������ʽ���㣻
��2�����ݡ��ȹ���ƽ����ֵ�������¶ȣ�Z�����ʵ���Ũ������ƽ��������Ӧ�����ƶ���
���
�⣺��1����ˮ�д���NH3?H2O?NH4++OH-����ˮϡ�ͣ��ٽ�һˮ�ϰ��ĵ��룬ƽ�����������ƶ�����n��NH4+����n��OH-������c��OH-����С��c��H+������������ʵĵ���ƽ�ⳣ�����䣬ˮ�����ӻ��������䣬�ʴ�Ϊ��bd��
��2�����ص����������õ��ӵĻ�ԭ��Ӧ���ںϳɰ��У������õ��ӣ�����������ӦΪ��N2+6H++6e-=2NH3���ʴ�Ϊ��N2+6H++6e-=2NH3��
��3�����ɱ��������ж������¶�ƽ�����������ƶ������H��0���������ʵľۼ�״̬�жϡ�S���ʴ�Ϊ����������
����֪��N2��g��+3H2��g��?2NH3��g����H=-92.4kJ/mol��������ȼ����285.8kJ/mol����Ӧ���Ȼ�ѧ����ʽΪ��H2��g��+
O2��g��=H2O��l����H=-285.8kJ/mol
�������Ȼ�ѧ����ʽ��ȥ�����ϲ����١�2+�ڡ�6�õ��Ȼ�ѧ����ʽΪ��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530kJ/mol��
�ʴ�Ϊ��+l530kJ/mol��
��1���¶�ΪT0ʱ��X�����ʵ���Ũ�ȵı仯��=��0.3-0.05��mol/L=0.25mol/L��
Y�����ʵ���Ũ�ȵı仯��=��0.4-0.15��mol/L=0.25mol/L��
Z�����ʵ���Ũ�ȵı仯��0.5-0��mol/L=0.5mol/L���÷�Ӧ����ʽΪX��g��+Y��g��?2Z��g����
���Է�����Ӧʱ�������ʵķ�Ӧ���ʴ�С��ϵΪ��2v��X��=2v��Y��=v��Z������Ӧ�Ļ�ѧ����ʽΪ��X��g��+Y��g��?2Z��g��
����ͼ���֪��c��X��=0.05mol/L��c��Y��=0.15mol/L��c��Z��=0.5mol/L��
K=
=
=33.3
�ʴ�Ϊ��33.3��
��2�����ݡ��ȹ���ƽ����ֵ�������¶ȣ�Z�����ʵ���Ũ��������ͼ��Ϊ��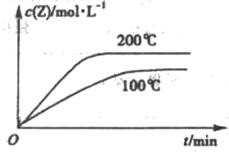 ��
��
�ʴ�Ϊ�� ��
��
��2�����ص����������õ��ӵĻ�ԭ��Ӧ���ںϳɰ��У������õ��ӣ�����������ӦΪ��N2+6H++6e-=2NH3���ʴ�Ϊ��N2+6H++6e-=2NH3��
��3�����ɱ��������ж������¶�ƽ�����������ƶ������H��0���������ʵľۼ�״̬�жϡ�S���ʴ�Ϊ����������
����֪��N2��g��+3H2��g��?2NH3��g����H=-92.4kJ/mol��������ȼ����285.8kJ/mol����Ӧ���Ȼ�ѧ����ʽΪ��H2��g��+
| 1 |
| 2 |
�������Ȼ�ѧ����ʽ��ȥ�����ϲ����١�2+�ڡ�6�õ��Ȼ�ѧ����ʽΪ��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530kJ/mol��
�ʴ�Ϊ��+l530kJ/mol��
��1���¶�ΪT0ʱ��X�����ʵ���Ũ�ȵı仯��=��0.3-0.05��mol/L=0.25mol/L��
Y�����ʵ���Ũ�ȵı仯��=��0.4-0.15��mol/L=0.25mol/L��
Z�����ʵ���Ũ�ȵı仯��0.5-0��mol/L=0.5mol/L���÷�Ӧ����ʽΪX��g��+Y��g��?2Z��g����
���Է�����Ӧʱ�������ʵķ�Ӧ���ʴ�С��ϵΪ��2v��X��=2v��Y��=v��Z������Ӧ�Ļ�ѧ����ʽΪ��X��g��+Y��g��?2Z��g��
����ͼ���֪��c��X��=0.05mol/L��c��Y��=0.15mol/L��c��Z��=0.5mol/L��
K=
| c2(Z) |
| c(X)c(Y) |
| (0.5mol/L)2 |
| 0.05mol/L��0.15mol/L |
�ʴ�Ϊ��33.3��
��2�����ݡ��ȹ���ƽ����ֵ�������¶ȣ�Z�����ʵ���Ũ��������ͼ��Ϊ��
 ��
���ʴ�Ϊ��
 ��
��
���������⿼���˻�ѧƽ��ļ��㣬Ӱ��ƽ������ط������缫��Ӧʽ����д����˹���ɵ�Ӧ�ã�����Ƕȹ㣬��Ŀ�ۺ���ǿ����ȷ����ͼ��ʱ���á��ȹ���ƽ����ֵ�����ж������������Դ�С����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
�������ʿ���ͨ�����Ϸ�Ӧ�Ƶõ��ǣ�������
��FeCl3��FeCl2��CuS ��FeS ��Fe��OH��3��
��FeCl3��FeCl2��CuS ��FeS ��Fe��OH��3��
| A���٢ڢܢ� | B���٢ڢۢܢ� |
| C���٢� | D���٢ܢ� |
����������ȷ���ǣ�������
A�� ʵ������ͼ��ʾװ����ȡ��ϩ |
| B����ˮ�������c��H+��=10-13mol?L-1����Һ�У�Na+��ClO-��K+��I-һ���ܴ������� |
| C����������Ҫ�ɷ��Ǹ�֬������ |
| D��ij�¶���Fe��OH��3��KSP=4��10-38������¶��£�������Һ��c��OH-��=2��10-19 mol?L-1 |
����˵���в���ȷ���ǣ�������
| A�����ά��������ά��ͭ����ά��������ά�����ɷֶ������� |
| B��������ˮ��������ע��Һ�����ܲ��������ЧӦ�������ڽ��� |
| C����������ǿ����ڲⶨ������Ĺ����š�1H�˴Ź����ǿ�ȷ��H�����Ļ�ѧ���� |
| D���ý��ݹ����������Һ�Ĺ���������ˮ���ͷŵ���ϩ���ɵ���ˮ�����ʵ�Ŀ�� |
ͨ�����ƻ�ı䷴Ӧ�������Լӿ졢����������ֹ��Ӧ�Ľ��У�ʹ��ѧ��Ӧ��������������������������������и�ͼ��ʾ�Ĵ�ʩ�У���Ϊ�˼ӿ컯ѧ��Ӧ���ʵ��ǣ�������
A�� ���ű������� |
B�� �����̿�� |
C�� ������ú¯�� |
D�� ľͷ���߸� |
�������أ��ŵ�ʱ���ܷ�ӦΪ��Fe+Ni2O3+3H2O
Fe��OH��2+2Ni��OH�� 2�����йظõ�ص�˵������ȷ���ǣ�������
| �ŵ� |
| ��� |
| A����صĵ��ҺΪ������Һ������ΪNi2O3������ΪFe |
| B����طŵ�ʱ��������ӦΪFe+2OH--2e-�TFe��OH��2 |
| C����س������У�����������Һ��pH���� |
| D����س��ʱ��������ӦΪ2Ni��OH��2+2OH--2e-�TNi2O3+3H2O |
��ѧ��������������������أ�����˵����ȷ���ǣ�������
| A���ֽ�������������֡�ʯ���ߡ�̼��ά��ǿ�մɶ��dz����ĸ��ϲ��� |
| B�������ʡ��������ᡢPVC�����ۡ���֬�����ɸ߷�����ɵ����� |
| C��SiO2�ƳɵIJ�����ά�����ڵ�������ǿ������������ͨѶ���� |
| D��ú��������Һ�������������̺�ɱ�Ϊ�����Դ������ú�ۺ����õ���Ҫ���� |
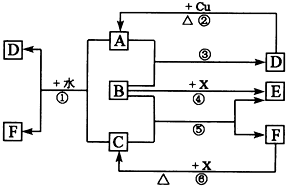 ���и�����Ϊ��ѧ��ѧ�г������ʣ�����A��C��E��FΪ���壬B��DΪ��ɫҺ�壬D��һ����Ҫ�Ļ���ԭ�ϣ�F��Ũ��Һ��X����ͨ������ʵ�����Ʊ�����C��X��һ�ֺ�ɫ��ĩ��B��������18�����ӣ�A���γ��������Ҫ���壮��Ӧ�в�������������ȥ��
���и�����Ϊ��ѧ��ѧ�г������ʣ�����A��C��E��FΪ���壬B��DΪ��ɫҺ�壬D��һ����Ҫ�Ļ���ԭ�ϣ�F��Ũ��Һ��X����ͨ������ʵ�����Ʊ�����C��X��һ�ֺ�ɫ��ĩ��B��������18�����ӣ�A���γ��������Ҫ���壮��Ӧ�в�������������ȥ��