题目内容
7.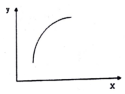 一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(S)+CO(g)?MgO(S)+CO2(g)+SO2(g)△H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(S)+CO(g)?MgO(S)+CO2(g)+SO2(g)△H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )| 选项 | x | y |
| A | SO2的浓度 | 平衡常数K |
| B | 温度 | 容器内混合气体的密度 |
| C | CO的物质的量 | CO2与CO的物质的量之比 |
| D | MgSO4的质量(忽略体积) | CO的转化率 |
| A. | A | B. | B | C. | C | D. | D |
分析 该反应是一个反应前后气体体积增大的吸热反应,
A.若x是二氧化硫的浓度,y是平衡常数,平衡常数只与温度有关,与物质浓度无关;
B.若x是温度,y是容器内混合气体的密度,升高温度,平衡向吸热反应方向移动;
C.若x是CO的物质的量,y是CO2与CO的物质的量之比,增大CO的物质的量,平衡向正反应方向移动,但加入的CO量大于CO转化的量;
D.若x是MgSO4的质量,y是CO的转化率,硫酸镁是固体,其质量不影响平衡移动.
解答 解:A.若x是二氧化硫的浓度,y是平衡常数,平衡常数只与温度有关,与物质浓度无关,增大二氧化硫浓度,温度不变,平衡常数不变,故A错误;
B.若x是温度,y是容器内混合气体的密度,升高温度,平衡向吸热反应方向正反应方向移动,气体的质量增大,容器体积不变,则容器内气体密度增大,所以符合图象,故B正确;
C.若x是CO的物质的量,y是CO2与CO的物质的量之比,增大CO的物质的量,平衡向正反应方向移动,但加入的CO量大于CO转化的量,所以增大CO的物质的量,CO2与CO的物质的量之比应该减小,故C错误;
D.若x是MgSO4的质量,y是CO的转化率,硫酸镁是固体,其质量不影响平衡移动,所以增大硫酸镁的质量,CO的转化率不变,故D错误.
故选B.
点评 本题考查图象分析,为高考常见题型和高频考点,侧重考查学生分析问题能力,明确纵横坐标的含义是解本题关键,注意:所有的平衡常数只有温度有关,易错选项C,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.下列说法不正确的是( )
| A. | 欲检验蔗糖水解产物是否具有还原性,不可以向水解后的溶液中直接加入新制的Cu(OH)2并加热 | |
| B. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 | |
| C. | 醋酸和硬脂酸互为同系物,C6H14和C9H20也一定互为同系物 | |
| D. | 迷迭香酸的结构为 它可以发生酯化、水解、加成等反应 它可以发生酯化、水解、加成等反应 |
2.甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备CH3OH(g).已知某些化学键的键能数据如表:
请回答下列问题:
(1)已知CO中的C与O之间为叁键连接,则工业制备CH3OH(g)的热化学方程式为CO(g)+2H2(g)?CH3OH (g)△H=-116 kJ•mol-1.
(2)在恒温恒容时,下列说法中能表明上述反应达到平衡状态的有ABD.
A.CO的物质的量不再变化B.v(H2)正=2v(CH3OH)逆
C.混合气体的密度不再变化D.混合气体的平均相对分子质量不再变化
(3)某研究小组在初始投料量相同的条件下,分别在250℃、300℃、350℃模拟以上工业生产进行实验,测定不同温度下CO的平衡转化率与压强的关系如图1所示.(A、B、C分别表示不同温度)

①TC=350℃;KA>KB(填“>”、“<”或“=”)
②实际生产时,通常选择温度为A℃、压强1.3×104kPa左右,选择此压强的理由是此压强下CO的转化率已较高,再增大压强转化率提高不大且会增加生产成本.
(4)如图2,常温下,利用甲醇燃料电池电解100mL 0.1食盐水,电解一段时间后,收集到氢气0.224L(已换算成标况下,忽略电解前后溶液体积的变化).
①电解后恢复至常温,U型管中溶液的pH=13(忽略Cl2与NaOH的反应)
②继续电解一段时间,将燃料电池中产生的0.1mol CO2通入到含有0.15mol NaOH的溶液中,则所得溶液中所有离子的浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
(1)已知CO中的C与O之间为叁键连接,则工业制备CH3OH(g)的热化学方程式为CO(g)+2H2(g)?CH3OH (g)△H=-116 kJ•mol-1.
(2)在恒温恒容时,下列说法中能表明上述反应达到平衡状态的有ABD.
A.CO的物质的量不再变化B.v(H2)正=2v(CH3OH)逆
C.混合气体的密度不再变化D.混合气体的平均相对分子质量不再变化
(3)某研究小组在初始投料量相同的条件下,分别在250℃、300℃、350℃模拟以上工业生产进行实验,测定不同温度下CO的平衡转化率与压强的关系如图1所示.(A、B、C分别表示不同温度)

①TC=350℃;KA>KB(填“>”、“<”或“=”)
②实际生产时,通常选择温度为A℃、压强1.3×104kPa左右,选择此压强的理由是此压强下CO的转化率已较高,再增大压强转化率提高不大且会增加生产成本.
(4)如图2,常温下,利用甲醇燃料电池电解100mL 0.1食盐水,电解一段时间后,收集到氢气0.224L(已换算成标况下,忽略电解前后溶液体积的变化).
①电解后恢复至常温,U型管中溶液的pH=13(忽略Cl2与NaOH的反应)
②继续电解一段时间,将燃料电池中产生的0.1mol CO2通入到含有0.15mol NaOH的溶液中,则所得溶液中所有离子的浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
12.目前各国排入空气中的CO2逐年增加,对此科学家最担心是( )
| A. | 会形成酸雨,造成森林大面积死亡 | |
| B. | 会使地球温度升高,冰川融化,生态失衡 | |
| C. | 会使人体吸进大量二氧化碳,损害健康 | |
| D. | 会使石灰岩大量溶解,破坏自然风光 |
19.下列分子中每个原子均满足8e-稳定结构的是( )
| A. | CH4 | B. | HClO | C. | N2 | D. | PCl5 |
 在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度升高,混合气体的颜色变深.
在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度升高,混合气体的颜色变深.