题目内容
16.硒和硫是同一主族元素,二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se.完成下列填空:(1)Se和浓HNO3反应的氧化产物为H2SeO3还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1,写出Se和浓HNO3的反应方程式:Se+2HNO3(浓)=SeO2+NO↑+NO2↑+H2O.
(2)已知:Se+2H2SO4(浓)═2SO2↑+SeO2+2H2O;2SO2+SeO2+2H2O═Se+2SO42-+4H+则SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是H2SO4(浓)>SeO2>SO2.
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
①1 SeO2+4 KI+4 HNO3→1Se+2 I2+4 KNO3+2 H2O
②I2+2Na2S2O3→Na2S4O6+2NaI 配平方程式①,标出电子转移的方向和数目.
(4)实验中,准确称量SeO2样品0.1500g,消耗了0.2000mol/L的Na2S2O3溶液25.00mL,所测定的样品中SeO2的质量分数为92.50%.
分析 (1)利用题中信息可知Se与浓HNO3反应,Se被氧化为+4价的H2SeO3,HNO3还原为NO与NO2,利用电子守恒和限定条件(生成NO与NO2的物质的量之比为1:1,即二者计量系数比为1:1)可得方程式;
(2)在氧化还原反应中,氧化剂的氧化性强于氧化产物的,而还原剂的还原性强于还原产物的;
(3)反应①中I-失去电子生成I2,共升高2价,SeO2中+4价Se得到单质还原为单质Se,共降低4价,化合价升降最小公倍数为4,进而确定各物质的量的系数配平方程式,确定转移电子数目,标出电子转移的方向和数目;
(4)根据反应的方程式可知,SeO2~2I2~4Na2S2O3,根据n=cV计算消耗的n(Na2S2O3),根据关系式计算样品中n(SeO2),再根据m=nM计算SeO2的质量,进而计算样品中SeO2的质量分数.
解答 解:(1)利用题中信息可知Se与浓HNO3反应,Se被氧化为+4价的H2SeO3,HNO3还原为NO与NO2,生成NO与NO2的物质的量之比为1:1,即二者计量系数比为1:1,令二者系数为1,根据电子转移守恒可知,Se的系数为$\frac{1×3+1×1}{4}$=1,故反应方程式为:Se+2HNO3(浓)=SeO2+NO↑+NO2↑+H2O,
故答案为:Se+2HNO3(浓)=SeO2+NO↑+NO2↑+H2O;
(2)在氧化还原反应中,氧化剂的氧化性强于氧化产物的,所以根据反应的方程式可知,SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是H2SO4(浓)>SeO2>SO2,
故答案为:H2SO4(浓)>SeO2>SO2;
(3)反应①中I-失去电子生成I2,共升高2价,SeO2中+4价Se得到单质还原为单质Se,共降低4价,化合价升降最小公倍数为4,故KI的系数为4,I2的系数为2,SeO2、Se的系数都是1,KNO3的系数为4,H2O的系数为2,配平并标出电子转移的方向和数目为: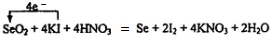 ,
,
故答案为:1,4,4,1,2,4,2;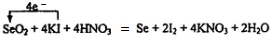 ;
;
(4)根据反应的方程式可知SeO2~2I2~4Na2S2O3,消耗的n(Na2S2O3)=0.2000 mol/L×0.025L=0.005mol,根据关系式计算样品中n(SeO2)=0.005mol×$\frac{1}{4}$=0.00125mol,故SeO2的质量为0.00125mol×111g/mol=0.13875g,所以样品中SeO2的质量分数为$\frac{0.13875g}{0.1500g}$×100%=92.50%,
故答案为:92.50%.
点评 本题考查氧化还原反应有关知识,涉及氧化性强弱比较、氧化还原反应配平、电子转移表示、氧化还原反应滴定计算等,难度中等,注意(4)中根据关系式的计算.

| A. | 用Cu与浓硝酸反应制NO2 | |
| B. | 用饱和NaHCO3溶液除去混在Cl2中的HCl气体 | |
| C. | 向AlCl3溶液中加入过量的NaOH溶液以制备Al(OH)3 | |
| D. | 用Cl2除去Fe2(SO4)3溶液中的少量FeSO4 |
①ClO3-+5Cl-+6H+═3Cl2+3H2O,
②2FeCl3+2KI═2FeCl2+2KCl+I2,
③2FeCl2+Cl2═2FeCl3,判断下列各微粒氧化能力由强到弱的顺序正确的是( )
| A. | Cl2>ClO3->Fe3+>I2 | B. | Cl2>ClO3->I2>Fe3+ | ||
| C. | ClO3->Cl2>Fe3+>I2 | D. | ClO3->Fe3+>Cl2>I2 |
 按如图装置进行电解实验:A极是铜锌合金,B极为纯铜.电解质中含有足量的铜离子.通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,溶液质量增加0.04g,则合金中Cu、Zn原子个数比为( )
按如图装置进行电解实验:A极是铜锌合金,B极为纯铜.电解质中含有足量的铜离子.通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,溶液质量增加0.04g,则合金中Cu、Zn原子个数比为( )| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 4:1 |
| A. | 1.25g/L | B. | 1.73g/L | C. | 1.96g/L | D. | 3.21g/L |
| A. | 标准状况下,22.4 L H2O 含有的分子数为 1 NA | |
| B. | 常温常压下,1.06 g Na2CO3 含有的 Na+离子数为 0.02 NA | |
| C. | 通常状况下,1 NA 个 CO2分子占有的体积为 22.4 L | |
| D. | 物质的量浓度为 0.5 mol/L 的 MgCl2溶液中,含有 Cl-个数为 1 NA |
 向200mL 6mol/L的盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定).
向200mL 6mol/L的盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定).