题目内容
某同学在鉴定某溶液中是否存在SO42-时向该溶液中滴加BaCl2溶液,发现有沉淀生成,于是就判断溶液中一定存在SO42-离子,他的判断是否正确?如果要求你来鉴定,你会怎样做?
考点:常见阴离子的检验
专题:物质检验鉴别题
分析:向溶液中滴加BaCl2溶液,发现有沉淀生成,该沉淀可能为氯化银、碳酸钡、亚硫酸钡等沉淀,不一定为硫酸钡,原溶液中不一定含有SO42-离子;然后根据检验硫酸根离子的方法进行检验硫酸根离子.
解答:
解:滴加BaCl2溶液,发现有沉淀生成,该白色沉淀可能为氯化银、碳酸钡等,不一定为硫酸钡,原溶液中不一定存在硫酸根离子,故该检验方法不正确;
正确检验方法为:先加入稀盐酸,没有产生沉淀,可以排除银离子、碳酸根、亚硫酸根的干扰,然后再加氯化钡溶液,若产生白色沉淀,证明有SO42-存在,否则不存在硫酸根离子,
答:不正确;取样,滴加稀盐酸,无明显现象,再滴加BaCl2溶液,看是否有不溶于水的白色沉淀生成.
正确检验方法为:先加入稀盐酸,没有产生沉淀,可以排除银离子、碳酸根、亚硫酸根的干扰,然后再加氯化钡溶液,若产生白色沉淀,证明有SO42-存在,否则不存在硫酸根离子,
答:不正确;取样,滴加稀盐酸,无明显现象,再滴加BaCl2溶液,看是否有不溶于水的白色沉淀生成.
点评:本题考查了硫酸根离子的检验方法判断,题目难度不大,试题侧重基础知识的考查,注意掌握常见离子的性质及检验方法,明确检验离子存在时,必须排除干扰离子,确保检验方案的严密性.

练习册系列答案
 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
用饱和的氯化铁溶液制取氢氧化铁胶体,正确的操作是( )
| A、将饱和氯化铁溶液滴入蒸馏水中即可 |
| B、将饱和氯化铁溶液滴入热水中,生成棕黄色液体即可 |
| C、将饱和氯化铁溶液滴入沸水中,并继续煮沸至生成红褐色液体即可 |
| D、将饱和氯化铁溶液滴入沸水中,并继续煮沸至生成红褐色沉淀即可 |
下列说法中正确的是( )
| A、摩尔是物质质量的单位,用“mol”表示 |
| B、标准状况下,物质的摩尔体积约为22.4 mol/L |
| C、阿伏伽德罗常数的真实值为6.02×1023 |
| D、物质的摩尔质量常用单位是“g/mol” |
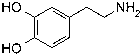 爱情是什么?化学家通过研究发现:大脑中心贮藏一种恋爱兴奋剂----多巴胺.当一对男女一见钟情或产生爱慕之情时,多巴胺就源源不断地分泌出来,于是爱情势不可挡地汹涌而出.多巴胺结构如图:
爱情是什么?化学家通过研究发现:大脑中心贮藏一种恋爱兴奋剂----多巴胺.当一对男女一见钟情或产生爱慕之情时,多巴胺就源源不断地分泌出来,于是爱情势不可挡地汹涌而出.多巴胺结构如图: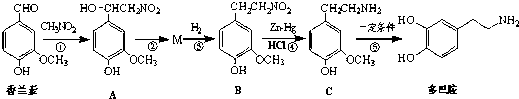
 氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用.
氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用.