题目内容
在标准状况下,5.6L的氢气和氯气的混合气体充分反应后,所得混合气体用100mL3.00mol/L的NaOH溶液恰好完全吸收,则:
(1)原混合气体中氯气的体积 L(标准状况下).
(2)所得溶液中Cl-的物质的量浓度为 .
(1)原混合气体中氯气的体积
(2)所得溶液中Cl-的物质的量浓度为
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:(1)在标准状况下,5.6L的氢气和氯气的混合气体充分反应后,所得混合气体用100mL3.00mol/L的NaOH溶液恰好完全吸收,所得溶液为NaCl溶液或NaCl、NaClO的混合溶液,由元素守恒可知:n(NaOH)=n(Cl原子),根据Cl原子守恒计算n(氯气),再根据V=nVm计算其体积;
(2)计算氢气的物质的量,根据电子转移守恒:n(Cl-)=2n(H2)+n(ClO-),据此计算溶液中n(Cl-),再根据c=
计算.
(2)计算氢气的物质的量,根据电子转移守恒:n(Cl-)=2n(H2)+n(ClO-),据此计算溶液中n(Cl-),再根据c=
| n |
| V |
解答:
解:(1)在标准状况下,5.6L的氢气和氯气的混合气体充分反应后,所得混合气体用100mL3.00mol/L的NaOH溶液恰好完全吸收,所得溶液为NaCl溶液或NaCl、NaClO的混合溶液,由元素守恒可知:n(NaOH)=n(Cl原子)=0.1L×3mol/L=0.3mol,根据Cl原子守恒可知n(Cl2)=0.15mol,故标况下氯气体积=0.15mol×22.4L/mol=3.36L,
故答案为:3.36;
(2)氢气的体积=5.6L-3.36L=2.24L,氢气物质的量=
=0.1mol,根据电子转移守恒:n(Cl-)=2n(H2)+n(ClO-)=2n(H2)+[n(NaOH)-n(Cl-)],即n(Cl-)=2×0.1mol+[0.3mol-n(Cl-)],解得n(Cl-)=0.25mol,故c(Cl-)=
=2.5mol/L,
故答案为:2.5mol/L.
故答案为:3.36;
(2)氢气的体积=5.6L-3.36L=2.24L,氢气物质的量=
| 2.24L |
| 22.4L/mol |
| 0.25mol |
| 0.1 L |
故答案为:2.5mol/L.
点评:本题考查混合物计算,侧重对解题方法技巧与学生思维能力的考查,转移利用原子守恒及电子转移守恒解答,难度中等.

练习册系列答案
相关题目
下列表达方式错误的是( )
A、甲烷的电子式 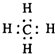 | ||
B、氟化钠的电子式 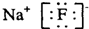 | ||
| C、硫离子的核外电子排布式 1s22s22p63s23p4 | ||
D、碳-12原子
|
下列关于热化学的说法正确的是( )
| A、需要加热才能发生的反应是吸热反应 |
| B、等量的金刚石和石墨固体分别完全燃烧,前者放出热量多,说明金刚石更稳定 |
| C、化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 |
| D、由热化学方程式 3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol可知,1molN2与3molH2放入密闭容器中,在催化剂的作用下反应得到氨气,将释放92kJ热量 |
 已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E.又知A原子的p轨道为半充满,其形成的简单氢化物的沸点是同主族非金属元素的氢化物中最高的.D原子得到一个电子后其3p轨道将全充满.B+离子比D原子形成的离子少一个电子层.C与B可形成BC型的离子化合物.E的原子序数为29.
已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E.又知A原子的p轨道为半充满,其形成的简单氢化物的沸点是同主族非金属元素的氢化物中最高的.D原子得到一个电子后其3p轨道将全充满.B+离子比D原子形成的离子少一个电子层.C与B可形成BC型的离子化合物.E的原子序数为29.
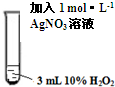

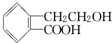 ,它可通过不同化学反应分别制得B、C和D三种物质.
,它可通过不同化学反应分别制得B、C和D三种物质.