题目内容
化学是一门以实验为基础的学科,熟练使用中学化学实验中的常见仪器,熟悉常见实验品是正确进行实验的基础.试回答以下问题:
现有如下仪器,用序号回答有关问题
①容量瓶 ②蒸馏烧瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥蒸发皿 ⑦分液漏斗
对允许加热的仪器,加热时必须垫石棉网的有 .
使用时必须检查是否漏水的有 .标有“0”刻度的有 .
Ⅱ实验室需要200mL1.0mol/L的NaOH溶液用于测定某盐酸样品的浓度.
(1)下列仪器中,配制NaOH溶液时必须用到的是(填写序号) .
①100mL量筒 ②烧杯 ③200mL容量瓶 ④250mL容量瓶⑤天平 ⑥胶头滴管 ⑦玻璃棒
(2)需要NaOH固体的质量是 .
(3)出现下列操作时,将使所配制的溶液浓度偏低的是 .
A.将烧杯内的NaOH溶液向容量瓶内转移时,部分溶液溅出瓶外
B.将烧杯内的NaOH溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
C.定容时仰视观察容量瓶刻度线和凹液面的最低点.
现有如下仪器,用序号回答有关问题
①容量瓶 ②蒸馏烧瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥蒸发皿 ⑦分液漏斗
对允许加热的仪器,加热时必须垫石棉网的有
使用时必须检查是否漏水的有
Ⅱ实验室需要200mL1.0mol/L的NaOH溶液用于测定某盐酸样品的浓度.
(1)下列仪器中,配制NaOH溶液时必须用到的是(填写序号)
①100mL量筒 ②烧杯 ③200mL容量瓶 ④250mL容量瓶⑤天平 ⑥胶头滴管 ⑦玻璃棒
(2)需要NaOH固体的质量是
(3)出现下列操作时,将使所配制的溶液浓度偏低的是
A.将烧杯内的NaOH溶液向容量瓶内转移时,部分溶液溅出瓶外
B.将烧杯内的NaOH溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
C.定容时仰视观察容量瓶刻度线和凹液面的最低点.
考点:间接加热的仪器及使用方法,计量仪器及使用方法,中和滴定
专题:实验题
分析:实验室中可直接加热的仪器有蒸发皿、试管、坩埚,垫石棉网可加热的有烧杯、烧瓶、锥形瓶等,不能加热的有集气瓶、广口瓶、细口瓶等;
能用来盛放液体,且有活塞的仪器使用时必须检查是否漏水;
一些计量仪器往往有0刻度;
Ⅱ(1)根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;
(2)先根据溶液的体积选取容量瓶的规格,再根据m=cVM求出溶质的质量,最后根据天平的精确度确定称量的质量;
(3)根据c=
分析操作对溶质的物质的量或对溶液的体积的影响判断.
能用来盛放液体,且有活塞的仪器使用时必须检查是否漏水;
一些计量仪器往往有0刻度;
Ⅱ(1)根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;
(2)先根据溶液的体积选取容量瓶的规格,再根据m=cVM求出溶质的质量,最后根据天平的精确度确定称量的质量;
(3)根据c=
| n |
| V |
解答:
解:蒸馏烧瓶和烧杯垫石棉网可加热;容量瓶、滴定管和分液漏斗能用来盛放液体,且有活塞,使用时必须检查是否漏水;滴定管有0刻度,在上方,故答案为:②⑤;①③⑦;③;
Ⅱ(1)配制步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,一般天平称量固体,把氯化钠倒入烧杯进行溶解(可用量筒量取水),冷却后转移到250mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器有玻璃棒、天平、药匙、烧杯、胶头滴管、100mL容量瓶,故答案为:②④⑤⑥⑦;
(2)因容量瓶的规格没有200mL,所以只能选取250mL的容量瓶,NaOH固体的质量m=nM=CVM=1.0mol?L-1×0.25L×40g/mol=10.0g,称量NaOH固体的质量是10.0g,故答案为:10.0g;
(3)A.将烧杯内的NaOH溶液向容量瓶内转移时,部分溶液溅出瓶外,导致溶质的物质的量偏小,配制的溶液浓度偏低,故A正确;
B.将烧杯内的NaOH溶液转移至容量瓶后,未洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,配制的溶液浓度偏低,故B正确;
C.定容时仰视观察容量瓶刻度线和凹液面的最低点,导致溶液的体积偏大,所以配制溶液的浓度偏低,故C正确;
故选:ABC.
Ⅱ(1)配制步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,一般天平称量固体,把氯化钠倒入烧杯进行溶解(可用量筒量取水),冷却后转移到250mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器有玻璃棒、天平、药匙、烧杯、胶头滴管、100mL容量瓶,故答案为:②④⑤⑥⑦;
(2)因容量瓶的规格没有200mL,所以只能选取250mL的容量瓶,NaOH固体的质量m=nM=CVM=1.0mol?L-1×0.25L×40g/mol=10.0g,称量NaOH固体的质量是10.0g,故答案为:10.0g;
(3)A.将烧杯内的NaOH溶液向容量瓶内转移时,部分溶液溅出瓶外,导致溶质的物质的量偏小,配制的溶液浓度偏低,故A正确;
B.将烧杯内的NaOH溶液转移至容量瓶后,未洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,配制的溶液浓度偏低,故B正确;
C.定容时仰视观察容量瓶刻度线和凹液面的最低点,导致溶液的体积偏大,所以配制溶液的浓度偏低,故C正确;
故选:ABC.
点评:本题主要考查了溶液的配制、化学方程式的计算,难度不大,关键清楚溶液配制的原理,通过c=
可以进行误差分析.
| n |
| V |

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
下列溶液中有关物质的量浓度关系不正确的( )
| A、pH=2的HA溶液与pH=12的MOH溶液以任意比混合:c(H+)+c(M+)=c(OH-)+c(A-) |
| B、pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3) |
| C、物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) |
| D、0.1 mol?L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(A2-)>c(H2A) |
将铁片和锌片放在盛有NaCl溶液(其中滴有酚酞)的表面皿中,如图所示,最先观察到变为红色的区域为( )
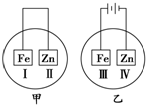

| A、Ⅰ和Ⅱ | B、Ⅰ和Ⅳ |
| C、Ⅱ和Ⅲ | D、Ⅱ和Ⅳ |
向碘水中加入酒精,观察到的现象是( )
A、 |
B、 |
C、 |
D、 |
下列关于0.2mol/LBa(NO3)2溶液正确的说法是( )
| A、2L溶液中含有Ba+离子0.2mol |
| B、2L溶液中含有NO3-离子0.2mol |
| C、0.5L溶液中Ba2+离子的物质的量浓度为0.2mol/L |
| D、0.5L溶液中NO3-离子的物质的量浓度为0.2mol/L |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1 mol NaHSO4晶体中离子总数为3NA |
| B、2.24 L 14CH4分子中所含中子数为0.8NA |
| C、0.1 L 3 mol?L-1的NH4NO3溶液中含有的NH4+数目为0.3NA |
| D、标准状况下,将FeSO4溶液置于空气中,被氧化的Fe2+为0.2NA,吸收O2为1.12 L |
根据下列反应判断还原剂的还原性由强到弱的顺序,正确的是( )
①Cl2+2KI═I2+2KCl
②2FeCl3+2HI═I2+2FeCl2+2HCl
③2FeCl2+Cl2═2FeCl3
④I2+SO2+2H2O═2HI+H2SO4.
①Cl2+2KI═I2+2KCl
②2FeCl3+2HI═I2+2FeCl2+2HCl
③2FeCl2+Cl2═2FeCl3
④I2+SO2+2H2O═2HI+H2SO4.
| A、SO2>I->Fe2+>Cl- |
| B、Cl2>Fe3+>I2>SO2 |
| C、Fe2+>Cl->I->SO2 |
| D、Cl->Fe2+>I->SO2 |