题目内容
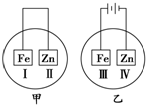
将铁片和锌片放在盛有NaCl溶液(其中滴有酚酞)的表面皿中,如图所示,最先观察到变为红色的区域为( )

| A、Ⅰ和Ⅱ | B、Ⅰ和Ⅳ |
| C、Ⅱ和Ⅲ | D、Ⅱ和Ⅳ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:第一个装置是原电池,Zn为负极,溶液中的氧气在Ⅰ处得电子生成OH-,所以Ⅰ处变红;第二个装置是电解池,铁为阳极,溶液中的H+在Ⅳ处得电子,破坏了锌片附近水的电离平衡,使得OH-浓度增大,所以Ⅳ处也变红.
解答:
解:甲图示是原电池,锌做负极,锌失电子形成锌离子,正极是Ⅰ,在正极上,O2+2H2O+4e-=4OH-;所以Ⅰ处变红;
乙图示是电解池,铁做阳极,铁失电子生成亚铁离子,锌做阴极,在阴极上,2H++2e-=H2↑,破坏了锌片附近水的电离平衡,使得OH-浓度增大,所以Ⅳ处也变红.
故选B.
乙图示是电解池,铁做阳极,铁失电子生成亚铁离子,锌做阴极,在阴极上,2H++2e-=H2↑,破坏了锌片附近水的电离平衡,使得OH-浓度增大,所以Ⅳ处也变红.
故选B.
点评:本题考查了原电池和电解池的工作原理的应用,为高频考点,侧重于学生的分析能力的考查,主要是电解反应的离子变化,难度不大.

练习册系列答案
 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
有一无色未知溶液中检验出有Ba2+、Ag+,同时又测得其酸性很强.某学生还要鉴定此溶液中是否大量存在①Cu2+ ②Fe3+ ③Cl- ④NO3- ⑤S2- ⑥CO32- ⑦NH4+ ⑧Mg2+ ⑨Al3+,而事实上有部分离子不用鉴定就能加以否定,你认为不必鉴定的是( )
| A、③⑤⑥⑦⑨ |
| B、①②⑤⑥⑧ |
| C、③④⑦⑧⑨ |
| D、①②③⑤⑥ |
实验室制取少量N2常利用的反应是NaNO2+NH4Cl
NaCl+N2↑+2H2O,关于该反应的说法正确的是( )
| ||
| A、NaNO2是氧化剂 |
| B、生成1molN2时转移的电子为6mol |
| C、NH4Cl中的N元素被还原 |
| D、N2既是氧化剂又是还原剂 |
有关能量的判断或表示方法正确的是( )
| A、由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,可知:含1mol CH3COOH的溶液与含1mol NaOH的溶液混合,放出热量等于57.3 kJ |
| B、等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
| C、从C(S、石墨)=C(S、金刚石)△H=+1.9kJ/mol,可知石墨比金刚石更稳定 |
| D、2gH2完全燃烧生成液态水放出285.8kJ热量,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2 H2O(l)△H=-285.8kJ/mol |
下列叙述中,正确的是( )
| A、硫酸的摩尔质量是98g |
| B、1mol N2的质量是28g/mol |
| C、阿伏加德罗常数是6.02×1023 |
| D、标准状况下,气体的摩尔体积约为22.4L/mol |