题目内容
18.把NaHCO3和Na2CO3•10H2O的混合物9.58g溶于水配成500mL溶液,其中Na+浓度为0.2mol•L-1;若把等质量的固体混合物加热至恒重,残留固体的质量为( )| A. | 1.06g | B. | 2.63g | C. | 3.6g | D. | 5.3g |
分析 固体混合物加热至恒重时,剩余固体为Na2CO3,根据Na元素守恒计算出剩余固体的物质的量,进而计算质量.
解答 解:固体混合物加热至恒重时,剩余固体为Na2CO3,
500mL溶液,其中c(Na+)═0.2mol•L-1.
则n(Na+)═0.5L×0.2mol•L-1=0.1mol,
n(Na2CO3)=0.05mol,
m(Na2CO3)=0.05mol×106g/mol=5.3g,
故选D.
点评 本题考查混合物的计算,题目难度不大,注意加热后剩余固体的成分,根据质量守恒计算.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
13.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 6.8g液态KHSO4中含有0.1NA个阳离子 | |
| B. | NA个Fe(OH)3胶体粒子形成的纳米材料的质量为107g | |
| C. | 等体积等密度的N2和CO所含分子数相同 | |
| D. | 含NA个Na+的Na2O溶解于水1L水中,Na+的物质的量浓度为1mol•L-1 |
3.如图危险标志对应正确的是( )
| A. |  烧碱 | B. |  甲烷 | C. |  酒精 | D. |  白磷 |
10.下列叙述正确的是( )
| A. | 固态氯化钠不导电,所以NaCl是非电解质 | |
| B. | 氨气的水溶液能导电,所以氨气是电解质 | |
| C. | SO3溶于水能导电,是因为SO3在水中发生了电离 | |
| D. | 液态氯化氢不导电,但是HCl是电解质 |
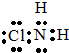 ,从物质结构的角度解释两者熔点相差较大的原因氯胺NH2Cl为分子晶体,NH4Cl为离子晶体,熔沸点离子晶体高于分子晶体.
,从物质结构的角度解释两者熔点相差较大的原因氯胺NH2Cl为分子晶体,NH4Cl为离子晶体,熔沸点离子晶体高于分子晶体. 如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: (1)纯净物根据其组成和性质可进行如图分类:
(1)纯净物根据其组成和性质可进行如图分类: