题目内容
13.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 6.8g液态KHSO4中含有0.1NA个阳离子 | |
| B. | NA个Fe(OH)3胶体粒子形成的纳米材料的质量为107g | |
| C. | 等体积等密度的N2和CO所含分子数相同 | |
| D. | 含NA个Na+的Na2O溶解于水1L水中,Na+的物质的量浓度为1mol•L-1 |
分析 A、求出KHSO4的物质的量,然后根据1molKHSO4中含1mol钾离子来分析;
B、一个氢氧化铁胶粒是多个氢氧化铁的聚集体;
C、氮气和CO的摩尔质量相同;
D、将氧化钠溶于1L水后,溶液体积大于1L.
解答 解:A、6.8gKHSO4的物质的量为0.05mol,而1molKHSO4中含1mol阳离子,故0.05mol中含0.05mol阳离子即0.05NA个,故A错误;
B、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故NA个氢氧化铁胶粒中含有的氢氧化铁的个数大于NA个,质量大于107g,故B错误;
C、等体积等密度的两气体的质量相同,而氮气和CO的摩尔质量相同,根据N=$\frac{m}{M}{N}_{A}$可知,分子个数相同,故C正确;
D、将氧化钠溶于1L水后,溶液体积大于1L,故溶液中的钠离子的浓度小于1mol/L,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
4.如表为元素周期表中的一部分,表中列出10种元素在周期表中的位置,按要求回答下列问题.
(1)化学性质最不活泼的元素是氩(填名称).
(2)元素①的单质在氧气中燃烧,生成的氧化物的化学式是CO2.
(3)第3周期主族元素中,元素原子半径最小的是Cl(填元素符号).
(4)元素⑨的单质和石灰乳作用可制取漂白粉,该反应的化学方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
(5)元素④的原子最外层电子数为7.
(6)元素⑦的氧化物常用于制造光导纤维(填一种高性能的现代通讯材料的名称).
(7)元素⑧、⑨中,化学性质较不活泼的元素是S(填元素符号),氢化物较稳定的是HCl(填化学式).
(8)元素②的氢化物化学式NH3,元素⑨的最高价氧化物的水化物的化学式HClO4
(9)元素⑤的氢氧化物和稀盐酸反应的化学方程式NaOH+HCl=NaCl+H2O.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素①的单质在氧气中燃烧,生成的氧化物的化学式是CO2.
(3)第3周期主族元素中,元素原子半径最小的是Cl(填元素符号).
(4)元素⑨的单质和石灰乳作用可制取漂白粉,该反应的化学方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
(5)元素④的原子最外层电子数为7.
(6)元素⑦的氧化物常用于制造光导纤维(填一种高性能的现代通讯材料的名称).
(7)元素⑧、⑨中,化学性质较不活泼的元素是S(填元素符号),氢化物较稳定的是HCl(填化学式).
(8)元素②的氢化物化学式NH3,元素⑨的最高价氧化物的水化物的化学式HClO4
(9)元素⑤的氢氧化物和稀盐酸反应的化学方程式NaOH+HCl=NaCl+H2O.
1.相同物质的量浓度的NaCl、MgCl2、AlCl3三种溶液的体积比是1:1:1,则三种溶液中氯离子的物质的量之比为( )
| A. | 1:2:3 | B. | 3:2:1 | C. | 1:1:1 | D. | 6:3:2 |
8.设NA为阿伏加德罗常数的值,下列有关说法不正确的是( )
| A. | 标准状况下,48gO3含有的氧原子数为3NA | |
| B. | 1molOH-离子中含电子数目为10NA | |
| C. | 0.2mol•L-1的NaCl溶液中含有的Na+数目为0.2NA | |
| D. | 常温常压下,33.6LCO中含有的原子数小于0.2NA |
18.把NaHCO3和Na2CO3•10H2O的混合物9.58g溶于水配成500mL溶液,其中Na+浓度为0.2mol•L-1;若把等质量的固体混合物加热至恒重,残留固体的质量为( )
| A. | 1.06g | B. | 2.63g | C. | 3.6g | D. | 5.3g |
5.下列意外事故处理或实验操作正确的是( )
| A. | 酒精灯不慎打翻着火用水浇灭 | |
| B. | 直接将浓硫酸倒入盛有水的烧杯中进行稀释 | |
| C. | 固体药品可用镊子或钥匙取用 | |
| D. | 蒸馏操作烧瓶可以直接用酒精灯加热 |
2.关于某无色溶液中所含离子的鉴别,下列判断正确的是( )
| A. | 加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl-存在 | |
| B. | 加入浓NaOH液并加热,产生可使湿润的蓝色石蕊试纸变红的气体,可确定有NH4+存在 | |
| C. | 加入盐酸,无明显现象,再加入BaCl2溶液,生成白色沉淀,可确定有SO42-存在 | |
| D. | 取该溶液进行焰色反应,火焰呈黄色,可确定有Na+,无K+ |
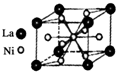 目前,利用金属或合金储氢已取得很大进展,先后发现了Ni、Mg、Fe基三个系列的储氢材料,如图是一种储氢密度超过液氢的镍基合金的晶胞结构图.
目前,利用金属或合金储氢已取得很大进展,先后发现了Ni、Mg、Fe基三个系列的储氢材料,如图是一种储氢密度超过液氢的镍基合金的晶胞结构图.