题目内容
13.已知MnO2是黑色难溶于水的固体,实验室制取氧气的反应为2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,充分反应后从剩余物中回收干燥的二氧化锰的正确操作顺序是( )| A. | 溶解、过滤、蒸发、洗涤 | B. | 溶解、蒸发、洗涤、过滤 | ||
| C. | 溶解、过滤、洗涤、干燥 | D. | 溶解、洗涤、过滤、干燥 |
分析 MnO2不溶于水,KCl溶于水,以此来解答.
解答 解:充分反应后混合物含KCl、MnO2,MnO2不溶于水,KCl溶于水,从剩余物中回收干燥的二氧化锰,则溶解、过滤、洗涤、干燥,
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离方法是解本题关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
3.在一定条件下,下列选项中括号内的物质能被完全消耗的是( )
| A. | 常温下将64g铜片投人过量浓硫酸中(铜片) | |
| B. | 向含有0.2molBa(OH)2和O.lmolNaOH的混合溶液中通人标况下3.36LCO2(CO2) | |
| C. | 向lOmL3mol•L-1的盐酸中加人5.6g铁(铁) | |
| D. | 向5.5gMn02粉末中加人20mL2mol•L-1双氧水(Mn02) |
1.用电解的方法可除去溶液中的NO3-,其原理如图所示,下列说法中正确的是( )
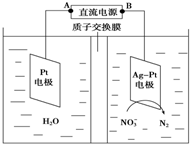

| A. | 铅蓄电池的B极为正极,电极材料为PbO2 | |
| B. | 铅蓄电池工作过程中负极质量增加 | |
| C. | 该电解池的阳极反应为:2 NO3-+6H2O-10e-═N2↑+12OH- | |
| D. | 若电解过程中转移10mol电子,则生成N2的体积为22.4L |
8.对于易燃、易爆、有毒的化学物质,往往会在其包装上贴危险警告标签,下面物质贴错标签的是( )
| A | B | C | D | |
| 物质的 化学式 | NaOH(浓) | C2H5OH(酒精) | H2SO4 (浓) | NH4NO3 |
| 危险警 告标签 |  |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
18.下列反应中,还原剂与氧化剂的质量比和物质的量之比不相同的是( )
| A. | 常温下用NaOH溶液吸收Cl2 | B. | Na在空气中燃烧 | ||
| C. | Na2O2吸收CO2 | D. | S在空气中燃烧 |
5.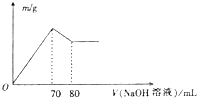 向100mL未知浓度的AlCl3和MgCl2的混合溶液中逐滴加入0.1 mol•L-1的NaOH溶液,生成沉淀的质量随加入NaOH溶液体积的变化关系如图所示,则AlCl3的浓度为( )
向100mL未知浓度的AlCl3和MgCl2的混合溶液中逐滴加入0.1 mol•L-1的NaOH溶液,生成沉淀的质量随加入NaOH溶液体积的变化关系如图所示,则AlCl3的浓度为( )
 向100mL未知浓度的AlCl3和MgCl2的混合溶液中逐滴加入0.1 mol•L-1的NaOH溶液,生成沉淀的质量随加入NaOH溶液体积的变化关系如图所示,则AlCl3的浓度为( )
向100mL未知浓度的AlCl3和MgCl2的混合溶液中逐滴加入0.1 mol•L-1的NaOH溶液,生成沉淀的质量随加入NaOH溶液体积的变化关系如图所示,则AlCl3的浓度为( )| A. | 0.005 mol•L-1 | B. | 0.01 mol•L-1 | C. | 0.2 mol•L-1 | D. | 0.1 mol•L-1 |
2.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 过氧化钠与水反应时,生成0.1mol氧气,转移电子数为0.2NA | |
| B. | 2L 0.5mol•L-1亚硫酸溶液中,含有的H+离子数为2NA | |
| C. | 常温常压下,1mol氦气含有的原子数为2NA | |
| D. | 标准状况下,11.2L水含有的分子数为0.5NA |