题目内容
14.A、B、C三只烧杯中,依次分别盛有NaOH溶液、KSCN溶液、煮沸的蒸馏水,各滴入饱和FeCl3溶液,试根据实验现象分别回答以下问题:(1)分别写出三只烧杯可能出现的现象A产生红褐色沉淀,B形成血红色溶液,C形成红褐色溶液.
(2)写出这三只烧杯中形成的分散系所属类型的名称:A悬浊液,B溶液,C胶体.
(3)写出A中形成分散系的离子反应方程式:Fe3++3OH-=Fe(OH)3↓.
(4)写出C中形成分散系的化学方程式:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl.
分析 氢氧化钠溶液中滴入FeCl3溶液会生成氢氧化铁沉淀;KSCN溶液中滴入FeCl3溶液会生成血红色溶液;煮沸的蒸馏水滴入FeCl3溶液会生成氢氧化铁胶体,以此解答该题.
解答 解:(1)氢氧化钠溶液中滴入FeCl3溶液会生成氢氧化铁红褐色沉淀;KSCN溶液中滴入FeCl3溶液会生成血红色溶液;煮沸的蒸馏水滴入FeCl3溶液会生成氢氧化铁胶体,为红褐色溶液,
故答案为:产生红褐色沉淀;形成血红色溶液;形成红褐色溶液;
(2)由(1)解答可知三种分散系分别为悬浊液、溶液、胶体,故答案为:悬浊液;溶液;胶体;
(3)氯化铁与氢氧化钠反应生成氢氧化铁沉淀,方程式为Fe3++3OH-=Fe(OH)3↓,故答案为:Fe3++3OH-=Fe(OH)3↓;
(4)氯化铁与沸水生成胶体,方程式为FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$ Fe(OH)3(胶体)+3HCl,故答案为:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$ Fe(OH)3(胶体)+3HCl.
点评 本题考查学生Fe(OH)3胶体的性质、制备以及胶体和溶液的鉴别等知识,为高频考点,侧重于学生的分析能力和实验能力的考查,注意知识的迁移和应用是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列叙述正确的是( )
| A. | 500mL 0.5mol•L-1 K2SO4溶液中,K+的总数为NA | |
| B. | 2L 0.5mol•L-1 K2SO4溶液中阴离子所带电荷数为NA | |
| C. | 18g H2O中含有10NA个质子 | |
| D. | 2L水中溶有80g的氢氧化钠,溶液的物质的量浓度为2mol•L-1 |
19.有下列3组有机物,①乙烯、苯、甲苯;②乙醇、乙酸、乙酸乙酯;③油脂、蛋白质、纤维素.根据你学过的知识,你认为下列说法错误的是( )
| A. | ①中有机物均可以发生还原反应 | |
| B. | ②中有机物可用饱和Na2CO3溶液鉴别 | |
| C. | ③中有机物均可以发生水解反应 | |
| D. | ③中有机物均属于高分子化合物 |
6.用pH大小表示溶液的酸碱性相对强弱有许多不足之处.因此,荷兰科学家Henk Van Lubeck引入了酸度(AG)的概念,即把电解质溶液中的酸度定义为c(H+)与c(OH-)比值的对数,用公式表示为AG=lg[$\frac{c({H}^{+})}{c(O{H}^{-})}$].常温下,在AG=-10的溶液中能大量共存的离子是( )
| A. | Ba2+、K+、Cl-、SO32- | B. | Na+、SiO32-、AlO2-、SO42- | ||
| C. | Na+、K+、HCO3-、S2- | D. | K+、NH4+、Fe3+、I- |
3.下列化学用语正确的是( )
| A. | CO2的结构式为O=C=O | B. | 乙烯的结构简式是C2H4 | ||
| C. | NaCl的电子式是Na:Cl: | D. | S原子的结构示意图: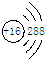 |
4.下列过程中涉及反应不属于氧化还原反应的是( )
| A. | Na2O2用作呼吸面具的供氧剂 | |
| B. | 工业上电解熔融状态的MgCl2制备Mg | |
| C. | 工业上利用合成氨实现人工固氮 | |
| D. | 实验室用NH4Cl和Ca(OH)2制备NH3 |

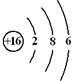 ,电子式表示化合物 C2D 的形成过程
,电子式表示化合物 C2D 的形成过程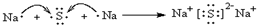 ;
;