题目内容
5.在指定溶液中,下列各组中的离子不能大量共存的是( )| A. | 由水电离出的c(H+)=1×10-12mol/L的溶液:Al3+、CH3COO-、NH4+、HCO3- | |
| B. | 试KSCN溶液变红的溶液:Na+、SO42-、H2O2、Cl- | |
| C. | 使酚酞变红的溶液:Ag(NH3)2+、CO32-、K+、S2- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12的溶液:K+、AlO2-、SiO32-、Na+ |
分析 A.由水电离出的c(H+)=1×10-12mol/L的溶液中存在大量氢离子或氢氧根离子,铝离子与碳酸氢根离子反应,醋酸根离子、碳酸氢根离子与氢离子反应,铵根离子、铝离子与氢氧根离子反应;
B.试KSCN溶液变红的溶液中存在铁离子,四种离子之间不反应,都不与铁离子反应;
C.使酚酞变红的溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
D.该溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应.
解答 解:A.由水电离出的c(H+)=1×10-12mol/L的溶液呈酸性或碱性,Al3+、HCO3-之间发生双水解反应,CH3COO-、HCO3-与氢离子反应,Al3+、NH4+与氢氧根离子反应,在溶液中一定不能大量共存,故A选;
B.试KSCN溶液变红的溶液中存在Fe3+,Na+、SO42-、H2O2、Cl-之间不发生反应,都不与Fe3+反应,在溶液中能够大量共存,故B不选;
C.使酚酞变红的溶液呈碱性,溶液中存在大量氢氧根离子,Ag(NH3)2+、CO32-、K+、S2-之间不发生反应,都不与氢氧根离子反应,在溶液中能够大量共存,故C不选;
D.该溶液呈碱性,溶液中存在大量氢氧根离子,K+、AlO2-、SiO32-、Na+之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故D不选;
故选A.
点评 本题考查离子共存的判断,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“能”共存,还是“不定”共存等.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
15.已知Na2SO3溶液可与K2Cr2O7溶液反应,现有0.1mol/L的Na2SO3溶液12mL,恰好与0.04mol/L的K2Cr2O7溶液10mL完全反应,通过计算确定Cr元素在还原产物中的化合价( )
| A. | +1 | B. | +3 | C. | +4 | D. | +5 |
16.下列表格中各项分类都正确的一组是( )
| 选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
| A | 纯碱 | 冰水混合物 | 液态KNO3 | 蔗糖 |
| B | CaO | 海水 | 铜 | 乙醇 |
| C | 明矾 | 铝合金 | AgCl | CO2 |
| D | 氢氧化钠 | 空气 | 氨水 | 食醋 |
| A. | A | B. | B | C. | C | D. | D |
13.甲、乙、丙、丁分别是BaCl2、NaOH、FeCl2、Al2(SO4)3、四种物质中的一种.若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,丁溶液滴入甲溶液时,无明显现象发生.据此可推断丙物质是( )
| A. | BaCl2 | B. | NaOH | C. | FeCl2 | D. | Al2(SO4)3 |
20.下列物质含有相同分子数的是( )
| A. | 1mol氯化氢和22.4升氮气 | |
| B. | 2molCO2和3molH2 | |
| C. | 在标准状况下16gO2和16gCH4 | |
| D. | 同温同压下,0.5mol氨气和14克CO气体 |
20.著名化学家徐光宪获得“国家最高科学技术奖”,以表彰他在稀土萃取理论方面作出的贡献.稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应.已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+.下列说法不正确的是( )
| A. | 铈(Ce)元素在自然界中主要以化合态形式存在 | |
| B. | 铈溶于氢碘酸的化学方程式可表示为:Ce+4HI═CeI4+2H2↑ | |
| C. | 用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+═Ce3++Fe3+ | |
| D. | 四种稳定的核素58136Ce、58138Ce、58140Ce、58142Ce,它们互称为同位素 |

 CH3Cl+HCl
CH3Cl+HCl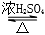 CH3COOCH2CH33+H2O
CH3COOCH2CH33+H2O 2CH3CHO+2H2O
2CH3CHO+2H2O