��Ŀ����
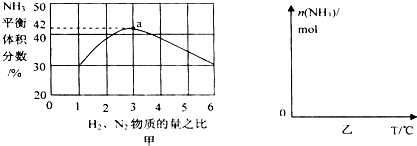
6���̶�������CO2����Ч��������Դ�������ٿ����е��������壮CO2�뻯�����Ӧ���ɻ�������뻯�����Ӧ���ɻ���������練Ӧ�ٺ͢���ʾ�������Լ������P��Ӧ������ʡ�ԣ���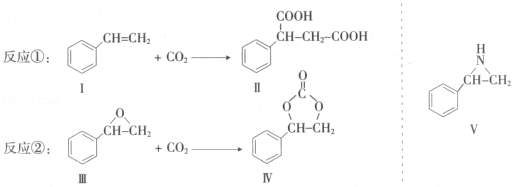
��1���������ķ���ʽΪC8H8��1mol��������ȫȼ��������10mol O2��
��2����
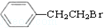 ͨ����ȥ��Ӧ�Ʊ���Ļ�ѧ����ʽΪ
ͨ����ȥ��Ӧ�Ʊ���Ļ�ѧ����ʽΪ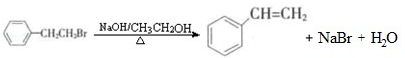 ��ע����Ӧ��������
��ע����Ӧ����������3���������C2H5OH������·���������Ӧ�����ɵ��л���Ľṹ��ʽΪ
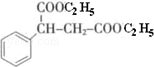 ��
����4����һ�������£�������V����CO2�������Ʒ�Ӧ�ڵķ�Ӧ���������ֻ������Ϊͬ���칹�壩����д����������һ�ֻ�����Ľṹ��ʽ��
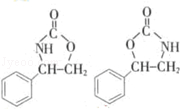 ��
����5����CO2���ƣ�COҲ�ܱ��̶������ã���һ�������£�CO��
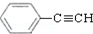 ��H2���߷�����Ӧ�����������뷴Ӧ�������ɻ�������͢��������ʽ��ΪC9H8O���Ҷ��ܷ���������Ӧ�����й��ڢ��͢���˵����ȷ����AB��˫ѡ������ĸ����
��H2���߷�����Ӧ�����������뷴Ӧ�������ɻ�������͢��������ʽ��ΪC9H8O���Ҷ��ܷ���������Ӧ�����й��ڢ��͢���˵����ȷ����AB��˫ѡ������ĸ����A�������ڷ����������� B������ʹ������Ȼ�̼��Һ��ɫ
C��������Na��Ӧ�ų�H2 D�� 1mol������������4mol H2�����ӳɷ�Ӧ��
���� ��1�����ݻ�����Ľṹ��ʽ��д����ʽ����CxHyȼ�պ�����Ϊx+$\frac{y}{4}$��
��2��±�����ܷ�����ȥ��Ӧ����ϩ����
��3������ʹ�����������Ӧ��������ˮ��
��4����Ӧ�ڵ�ʵ���Ƿ����ļӳɷ�Ӧ��
��5�������л���Ľṹ������֮��Ĺ�ϵ���лش�
��� �⣺��1�����л����Ľṹ��ʽ����д�������ʽΪ��C8H8��������CxHy������Ϊx+y/4���������Ϊ10mol���ʴ�Ϊ��C8H8��10��
��2��±���� ��ͨ����ȥ��Ӧ����ȥС�����廯�⣬����ʽΪ��
��ͨ����ȥ��Ӧ����ȥС�����廯�⣬����ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��3��1mol���к���2mol�Ȼ�����2molC2H5OH������·���������Ӧ���õ���Ӧ����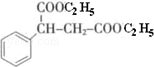 ���ʴ�Ϊ��
���ʴ�Ϊ��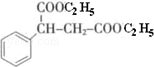 ��
��
��4��������V����CO2�������Ʒ�Ӧ�ڵķ�Ӧ����ԭ���ǣ�O=C=O�е�һ��̼�����Ͽ����л���Ͽ�̼�����ӳɣ������ּӳɷ�ʽ����ṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ����дһ�֣���
����дһ�֣���
��5�� �ķ���ʽΪC8H6����C9H8O��һ��CH2O�����Ҿ��ܷ���������Ӧ�������ɵĻ�������͢�����ȩ����˫�����ṹ��ʽ�ֱ�Ϊ
�ķ���ʽΪC8H6����C9H8O��һ��CH2O�����Ҿ��ܷ���������Ӧ�������ɵĻ�������͢�����ȩ����˫�����ṹ��ʽ�ֱ�Ϊ ��A��B��ȷ��1mol�����������к�ȩ����˫����1mol����������3mol����������������5mol����D�����л�����û�к��Ʒ�Ӧ�Ĺ����ţ���C���ʴ�Ϊ��AB��
��A��B��ȷ��1mol�����������к�ȩ����˫����1mol����������3mol����������������5mol����D�����л�����û�к��Ʒ�Ӧ�Ĺ����ţ���C���ʴ�Ϊ��AB��
���� ���⿼���л���ṹ�����ʡ��л����ƶϣ�Ϊ��Ƶ���㣬��ȷ�����ż������ʹ�ϵ�ǽⱾ��ؼ���֪�������л��ﷴӦ���ͼ���Ӧ�������ϼ��ͳɼ���ʽ����Ŀ�Ѷ��еȣ�

 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д� ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д�| A�� | ֱ��¶����սո� | B�� | ?���ܷ��� | ||
| C�� | ����ֱ���ŷ�β�� | D�� | ��ʯ����ȼ�� |
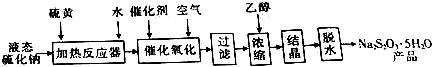
�ش��������⣺
��1����Ӧ����Na2S��S�����ʵ���֮��1��1��Ӧ�����ӷ���ʽΪS2-+S=2S2-����Ӧ������ȵ�Ŀ����ʹNa2S��S�ܳ�ַ�Ӧ
��2������ʱ���������[m��MnSO4����m��NiSO4•7H2O��=1��4]����ò�ͬ�¶�����ȫ��������ʱ�������
| ��Һ�¶�/�� | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| ������ȫ����ʱ��/h | 6 | 5.5 | 5.5 | 6 | 20 | 16 | 11 | 11 |
��3������ʱ����������Ҫ�ɷ�Ϊ��Һ̬����ԭ���е����ʣ�Ũ��ʱ���������Ҵ���Ŀ���Ǽ�СNa2S2O3���ܽ�ȣ�
| A�� | 14g��ϩ�ͱ�ϩ�Ļ�����У����й��õ��Ӷ���ĿΪ3NA | |
| B�� | 1mol�����С�C=C���ĸ���Ϊ3NA | |
| C�� | ��״���£�1L������ȼ�պ����ɵ���̬����ķ�����Ϊ$\frac{5}{22.4}$NA | |
| D�� | ��״���£�560mL����ͼ�ȩ�Ļ�������У����еĹ��õ��Ӷ���Ϊ0.1NA |
| A�� | �����¶ȣ�KW����pH���� | |
| B�� | ��ˮ�м��백ˮ��ƽ�����淴Ӧ�����ƶ���c��OH-������ | |
| C�� | ��ˮ�м��������Ȼ�泥�c��H+������ | |
| D�� | ��ˮ�м�����������CH3COONa��ƽ�����淴Ӧ�����ƶ���c��H+������ |
| A�� | Cl2��HCl | B�� | NO2��HNO3 | C�� | Fe2O3��Fe | D�� | SiO2��H2SiO3 |
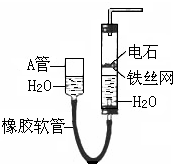 ��ͼ�е�ʵ��װ�ÿ�������ȡ��Ȳ������գ�
��ͼ�е�ʵ��װ�ÿ�������ȡ��Ȳ������գ� ��
��

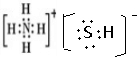 ��д��������Ӧ�Ļ�ѧ����ʽ��2NH4HS+O2$\frac{\underline{\;һ������\;}}{\;}$2NH3•H2O+2S��NH3�ķе����H2S������ΪNH3����֮�������һ�ֽ��������������
��д��������Ӧ�Ļ�ѧ����ʽ��2NH4HS+O2$\frac{\underline{\;һ������\;}}{\;}$2NH3•H2O+2S��NH3�ķе����H2S������ΪNH3����֮�������һ�ֽ��������������