题目内容
12.下列说法中正确的是( )| A. | 通常元素的化合价与其原子的质量数有密切的关系 | |
| B. | 已知铱的一种核素是${\;}_{77}^{191}$Ir,则其核内的中子数是114 | |
| C. | ${\;}_{6}^{14}$C和${\;}_{7}^{17}$N的质量数相同,但质子数不同,所以互称为同位素 | |
| D. | 钾的原子结构示意图为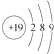 |
分析 A.元素的化合价与其最外层电子数有密切的关系;
B.元素符号左上角数字表示质量数、左下角数字表示质子数,中子数=质量数-质子数;
C.元素符号左上角数字表示质量数;
D.最外层电子数不能超过8个.
解答 解:A.元素的化合价与其最外层电子数有密切的关系,与质量数无关,故A错误;
B.该元素的质量数是191、质子数是77,中子数=质量数-质子数=191-77=114,故B正确;
C.${\;}_{6}^{14}$C和${\;}_{7}^{17}$N的质量数分别为14、17,故C错误;
D.钾的原子结构示意图为 ,故D错误.
,故D错误.
故选B.
点评 本题考查化合价、中子数的计算,同位素以及原子结构示意图等知识,明确质量数、质子数和中子数的关系是解本题关键,根据公式解答即可,题目难度不大.

练习册系列答案
相关题目
2.下列有关实验装置进行的相应实验,能达到实验目的是( )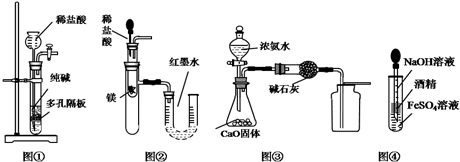

| A. | 用图①所示装置制取少量纯净的CO2气体 | |
| B. | 用图②所示装置验证镁和盐酸反应的热效应 | |
| C. | 用图③所示装置制取并收集干燥纯净的NH3 | |
| D. | 用图④装置制备Fe(OH)2并能保证较长时间观察到白色 |
7.元素的周期数等于( )
| A. | 电子层数 | B. | 原子量 | C. | 次外层电子数 | D. | 最外层电子数 |
17.1.52g 铜镁合金完全溶解于50mL 密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
| A. | 该合金中铜与镁的物质的量之比是2:1 | |
| B. | 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L | |
| C. | 得到2.54 g沉淀时,加入NaOH溶液的体积是60 mL | |
| D. | NO2和N2O4的混合气体中,NO2的体积分数是80% |
1.以下区别二氧化硫和二氧化碳气体的最好方法是( )
| A. | 通入澄清石灰水 | B. | 用湿润的蓝色石蕊试纸 | ||
| C. | 用品红溶液 | D. | 根据气体有无颜色 |
2.从化学看生活,你认为下列说法不合理的是( )
| A. | 镁铝合金质量轻、强度大,可用作高铁车厢材料 | |
| B. | 用纸制品、聚乳酸等物质来替代聚乙烯产品,以减少白色污染 | |
| C. | 明矾可用于水的消毒、杀菌 | |
| D. | 大量燃烧化石燃料,是造成雾霾天气的一种原因 |
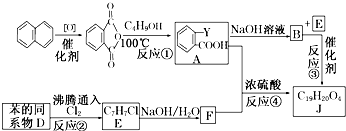
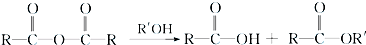
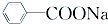 +RCl→
+RCl→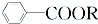 +NaCl;
+NaCl; .
. .
.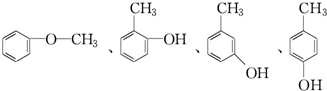 .
.