题目内容
20.标准状况下,往100mL 0.4mol/L的FeBr2溶液中通入一定体积的Cl2,充分反应后,溶液中有50%的Br-被氧化.则通入的氯气的体积是( )| A. | 0.448L | B. | 0.672L | C. | 0.896L | D. | 1.344L |
分析 还原性Fe2+>Br-,氯气先氧化亚铁离子,亚铁离子反应完毕,再氧化溴离子为Br2,根据电子转移守恒计算通入氯气物质的量,进而计算氯气体积.
解答 解:n(FeBr2)=0.4mol/L×0.1L=0.04mol,则n(Fe2+)=n(FeBr2)=0.04mol,n(Br-)=2n(FeBr2)=0.08mol,
还原性Fe2+>Br-,氯气先氧化亚铁离子,亚铁离子反应完毕,再氧化溴离子为Br2,溶液中有50%的Br-被氧化,则被氧化的Br-为0.04mol,根据电子转移守恒,通入氯气物质的量为$\frac{0.04mol×(3-2)+0.04mol×1}{2}$=0.04mol,则通入氯气的体积为0.04mol×22.4L/mol=0.896L,
故选:C.
点评 本题考查化学方程式计算,明确溶液中离子反应的先后顺序是解本题的关键,注意利用电子转移守恒计算解答.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
10.雾霾严重影响人们的生活与健康.某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-.某同学收集了该地区的雾霾,经必要的预处理后的试样溶液,设计并完成了如下的实验:
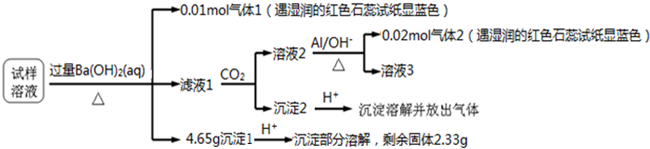
已知:3NO3-+8Al+5OH-+2H2O$\stackrel{△}{→}$3NH3+8AlO2-,根据以上的实验操作与现象,该同学得出的结论正确的是( )

已知:3NO3-+8Al+5OH-+2H2O$\stackrel{△}{→}$3NH3+8AlO2-,根据以上的实验操作与现象,该同学得出的结论正确的是( )
| A. | 沉淀2为氢氧化铝 | |
| B. | Cl-一定存在,且c(Cl?)≥0.05mol | |
| C. | 该试样溶液中一定存在的离子有NH4+、Mg2+、Al3+、SO42-和NO3- | |
| D. | 试样中可能存在Na+、Cl-、Al3+ |
11.铝和氢氧化钾都是重要的工业产品.工业品氢氧化钾的溶液中含有某些含氧酸杂质,可用离子交换膜法电解提纯.电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示,下列说法正确的( )

| A. | 阳极产生KOH | |
| B. | 阴极产生KOH | |
| C. | 大量H+ 通过离子交换膜从左侧到右侧 | |
| D. | 大量K+通过离子交换膜从右侧到左侧 |
8.现有三组溶液:①煤油和氯化钾溶液②35%的乙醇溶液③碘单质和氯化钠固体,分离以上各混合体系最合适的方法依次是( )
| A. | 分液、蒸馏、萃取 | B. | 萃取、蒸馏、升华 | C. | 分液、蒸馏、升华 | D. | 蒸馏、分液、萃取 |
15.将一定量的Na和Na2O2的混合物与足量的水反应,在标准状祝下得到1.008L混合气体,将混合气体收集并干燥后,用电火花引燃混合气恰好完全反应,则Na和Na2O2的物质的量之比为( )
| A. | 2:1 | B. | l:2 | C. | l:1 | D. | 3:l |
12.下列关于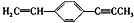 ,说法正确的是( )
,说法正确的是( )
 ,说法正确的是( )
,说法正确的是( )| A. | 最多只能有9个碳原子在同一平面上 | |
| B. | 有6个碳原子可能在同一直线上 | |
| C. | 最多有4个碳原子在同一直线上 | |
| D. | 所有原子一定都在同一平面上 |
9.若把周期表原先的主、副族号取消,由左到右按原顺序编为18列,如碱金属为第1列,稀有气体为第18列,按这个规定,下列说法不正确的是( )
| A. | 计算机芯片的组成元素位于第14列 | |
| B. | 第10列元素全部是金属元素 | |
| C. | 第18列元素单质全部是气体 | |
| D. | 只有第2列元素的原子最外层有2个电子 |
19.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.4g镁原子变成离子时,失去的电子数为0.3NA | |
| B. | 22.4L甲烷(CH4)所含的原子数为5NA | |
| C. | 98 g H2SO4和98 g H3PO4所含的氧原子数都是4NA | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA |
 将2.5g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
将2.5g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示: