题目内容
14.M为一种常见的液体试剂.下列物质在一定条件下可发生如图所示的转化关系.回答下列问题:
(1)写出淡黄色粉末和M反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑;
(2)若固体乙是硫化铝,则:①C的化学式是H2S,G的化学式是H2SO4;
②H溶解于A溶液的离子方程式是Al2O3+2OH-=AlO2+H2O;
(3)若白色沉淀D不能溶解于A溶液,气体C能使湿润的红色试纸变蓝,则固体乙的化学式可能是Mg3N2.
分析 M为一种常见的液体试剂,结合图中转化可知,淡黄色粉末为Na2O2,M为H2O,A为NaOH,气体B为O2,气体C可发生连续氧化反应,G为酸,且乙与水反应生成气体和沉淀,则固体乙可为Mg3N2或Al2S3,C为氨气或H2S,白色沉淀D为氢氧化镁或氢氧化铝,若C为H2S,E为SO2,F为SO3,G为H2SO4,以此来解答.
解答 解:M为一种常见的液体试剂,结合图中转化可知,淡黄色粉末为Na2O2,M为H2O,A为NaOH,气体B为O2,气体C可发生连续氧化反应,G为酸,且乙与水反应生成气体和沉淀,则固体乙可为Mg3N2或Al2S3,C为氨气或H2S,白色沉淀D为氢氧化镁或氢氧化铝,若C为H2S,E为SO2,F为SO3,G为H2SO4,
(1)淡黄色粉末和M反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(2)若固体乙是硫化铝,则:①C的化学式是H2S,G的化学式是 H2SO4,故答案为:H2S; H2SO4;
②H为氧化铝,A为NaOH,H溶解于A溶液的离子方程式是Al2O3+2OH-=AlO2+H2O,故答案为:Al2O3+2OH-=AlO2+H2O;
(3)若白色沉淀D不能溶解于A溶液,气体C能使湿润的红色试纸变蓝,D为氢氧化镁,C为氨气,则固体乙的化学式可能是Mg3N2,故答案为:Mg3N2.
点评 本题考查无机物的推断,为高频考点,涉及常见元素及其化合物知识的考查,把握元素化合物知识、反应与性质为解答的关键,侧重分析与推断能力的考查,注意乙为推断的难点,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列说法不正确的是( )
| A. | 乙烯在空气中燃烧时有黑烟,因此可以用燃烧法区别甲烷和乙烯 | |
| B. | 苯与浓硝酸在浓硫酸存在条件下加热发生取代反应 | |
| C. | 蛋白质溶液中加入饱和硫酸铵溶液,蛋白质发生变性 | |
| D. | 氨基酸能够以不同数目和顺序相结合形成结构复杂的多肽 |
5.下列反应不能用离子方程式“H++OH-=H2O”表示的是( )
| A. | H2SO4溶液与NaOH溶液混合 | B. | HCl气体通入Ca(OH)2溶液中 | ||
| C. | HNO3溶液与KOH溶液混合 | D. | NH4HSO4溶液与NaOH溶液混合 |
9.在强酸溶液中,下列各组离子能够大量共存的是( )
| A. | Mg2+、Ca2+、HCO3-、Cl- | B. | Fe2+、Ca2+、Cl-、NO3- | ||
| C. | K+、Fe2+、SO42-、Br- | D. | Na+、K+、SO42-、AlO2- |
19.下列有关图象正确的是( )
| A. | 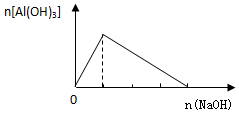 向AlCl3溶液中逐滴加入NaOH溶液 | |
| B. | 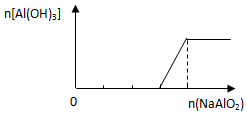 向稀盐酸中逐滴加入NaAlO2溶液 | |
| C. | 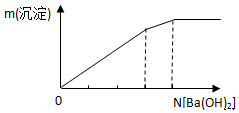 向明矾溶液中逐滴加入Ba(OH)2溶液 | |
| D. | 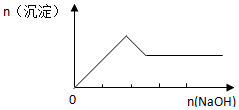 向Al2O3和Fe2O3的混合物中加入过量稀盐酸,向所得溶液中滴加NaOH的过程 |
6.下列各组离子一定能大量共存的是( )
| A. | 在强碱溶液中:Na+、K+、CO32-、NO3- | |
| B. | 在pOH=2的溶液中:NH4+、Na+、SO42-、AlO2- | |
| C. | 在pH=1的溶液中:K+、Ag+、Mg2+、Fe2+ | |
| D. | 水电离出来的c(H+)=1×10-13 mol•L-1的溶液:K+、HCO3-、Br-、Ba2+ |
4.有X、Y、Z、W、M五种原子序数增大的短周期元素,其中X、M同主族; Z+与Y2-具有相同的电子层结构,W是地壳中含量最多的金属,X与W的原子序数之和等于Y与Z的原子序数之和;下列序数不正确的是( )
| A. | X有多种同素异形体,而Y不存在同素异形体 | |
| B. | X、M均能与氯形成由极性键构成的XCl4、MCl4分子 | |
| C. | W的氧化物对应的水化物可与Z的最高价氧化物对应的水化物反应 | |
| D. | 离子半径大小:r(Y2-)>r(W3+) |
 对于反应2A+B?2C的反应过程中C的百分含量随温度的变化如图所示,则:
对于反应2A+B?2C的反应过程中C的百分含量随温度的变化如图所示,则: 现有部分元素的存在,性质和原子结构如下所述:
现有部分元素的存在,性质和原子结构如下所述: