题目内容
14.请按照官能团的不同对下列有机物进行分类:①CH3CH=CHCH3②CH≡CH③CH3CH2CH3④
 ⑤
⑤ ⑥
⑥ ⑦
⑦
⑧
 ⑨CCl2F2⑩CCl4⑪CH3CH2OH⑫
⑨CCl2F2⑩CCl4⑪CH3CH2OH⑫
其中:
(1)属于醛类物质的是⑤(填序号,下同).
(2)属于酯类物质的是⑧.
(3)属于芳香族化合物的是④⑫.
分析 (1)醛是醛基(-CHO)和烃基(或氢原子)连接而成的化合物.
(2)酯由羧酸与醇(酚)反应失水而生成的化合物,含有酯基;
(3)含苯环的化合物为芳香族化合物.据此分析.
解答 解:①CH3CH=CHCH3是官能团为碳碳双键的烃,故为烯烃;
②CH≡CH是官能团为碳碳三键的烃,故为炔烃;
③CH3CH2CH3是烷烃;
④ 是含苯环的化合物,故属于芳香化合物;
是含苯环的化合物,故属于芳香化合物;
⑤ 含醛基,故属于醛类;
含醛基,故属于醛类;
⑥ 的官能团为羰基,故属于酮类;
的官能团为羰基,故属于酮类;
⑦ 为甲酸,属于羧酸类;
为甲酸,属于羧酸类;
⑧ 的官能团为酯基,属于酯类;
的官能团为酯基,属于酯类;
⑨CCl2F2的官能团为卤素原子,故属于卤代烃;
⑩CCl4的官能团为卤素原子,故属于卤代烃;
⑪CH3CH2OH的官能团为-OH,且-OH连在链烃基上,故为醇类;
⑫ 是含苯环的化合物,故属于芳香化合物;
是含苯环的化合物,故属于芳香化合物;
(1)醛是醛基(-CHO)和烃基(或氢原子)连接而成的化合物,故⑤是醛类,故答案为:⑤.
(2)酯由羧酸与醇(酚)反应失水而生成的化合物,含有酯基,故⑧是酯类,故答案为:⑧;
(3)含苯环的化合物为芳香族化合物,故④⑫是芳香族化合物,故答案为:④⑫.
点评 本题考查了有机化合物的分类,涉及醇、酚、芳香烃、卤代烃、酸、酯类等物质的判断,难度不大,根据概念判断即可,注意把握好官能团.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.下列各说法正确的是( )
| A. | 电解精炼铜,阴极析出32g铜时,转移电子数一定大于NA | |
| B. |  图中K与M相连时,向U形试管中滴加铁氰化钾溶液,会在铁棒附件看到蓝色沉淀 | |
| C. | 金属铝很活泼,工业制备只能用电解熔融AlCl3的方法制备 | |
| D. | 电镀铜,阴、阳极质量差值增大6.4g时,转移电子为0.1NA |
9.硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示,下列说法错误的是( )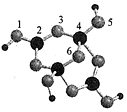

| A. | 在Xm-中,硼原子轨道的杂化类型有sp2、sp3 | |
| B. | 配位键存在于4、5原子之间 | |
| C. | m=3 | |
| D. | 硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有共价键、范德华力、氢键 |
19.氨水和盐酸是常见的化学试剂,可将氨气(NH3)、氯化氢气体分别溶于水制得.
(1)氨气的发生装置可以选择如图1中的A或B,反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,NH3•H2O$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(2)欲收集一瓶干燥的氨气,选择如图中的装置,其连接顺序为:发生装置→d→c→f→e→i(按气流方向,用小写字母表示).
(3)小华为探究氨气溶于水是否发生化学反应,设计并完成如表实验(填写表中空白):
(4)小明将滴有酚酞的稀氨水加热,观察到溶液颜色变浅,原因可能是氨水不稳定受热易分解生成氨气和水,导致溶液碱性减弱,则溶液颜色变浅.
(5)小芳将滴有石蕊的稀盐酸加热,溶液颜色无明显变化.为进一步研究,取稀盐酸分成2份:①未经加热;②加热煮沸一段时间后冷却,分别中和等量的氢氧化钠,消耗二者的质量:①>②,则稀盐酸经加热煮沸后浓度增大(填“增大”、“减小”或“不变”).为除去氯化钠溶液中的碳酸钠,小林设计了如图2方案:
你认为上述方案不合理(填“合理”或“不合理”),请分析:根据上述实验,加热煮沸无法除去溶液A中混有的过量氯化氢.改进方案:向含碳酸钠的氯化钠溶液中边逐滴加盐酸,边测定溶液的pH,至溶液呈中性即可(如合理,说明原因;如不合理,说明原因并设计改进方案).
(6)为研究氨气的还原性,小兰做了以下实验:
将(2)收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好).在一定温度如图3所示装置进行实验.

(1)氨气的发生装置可以选择如图1中的A或B,反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,NH3•H2O$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(2)欲收集一瓶干燥的氨气,选择如图中的装置,其连接顺序为:发生装置→d→c→f→e→i(按气流方向,用小写字母表示).
(3)小华为探究氨气溶于水是否发生化学反应,设计并完成如表实验(填写表中空白):
| 实验操作 | 实验现象及结论 |
| 将浸有酚酞溶液的滤纸干燥后,放入盛有干燥氨气的集气瓶中 | 无明显现象 |
| 将浸有酚酞溶液的滤纸湿润后,放入盛有干操氨气的集气瓶中 | 滤纸变红,说明氨气遇水形成溶液呈碱性 |
(5)小芳将滴有石蕊的稀盐酸加热,溶液颜色无明显变化.为进一步研究,取稀盐酸分成2份:①未经加热;②加热煮沸一段时间后冷却,分别中和等量的氢氧化钠,消耗二者的质量:①>②,则稀盐酸经加热煮沸后浓度增大(填“增大”、“减小”或“不变”).为除去氯化钠溶液中的碳酸钠,小林设计了如图2方案:
你认为上述方案不合理(填“合理”或“不合理”),请分析:根据上述实验,加热煮沸无法除去溶液A中混有的过量氯化氢.改进方案:向含碳酸钠的氯化钠溶液中边逐滴加盐酸,边测定溶液的pH,至溶液呈中性即可(如合理,说明原因;如不合理,说明原因并设计改进方案).
(6)为研究氨气的还原性,小兰做了以下实验:
将(2)收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好).在一定温度如图3所示装置进行实验.
| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中 | ①Y管中Y管中红棕色气体慢慢变浅,最后褪为无色 | ②反应的化学方程式 反应的化学方程式8NH3+6NO2 $\frac{\underline{\;催化剂\;}}{\;}$7N2+12H2O |
| 将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝聚 |
| 打开K2 | ③Z中的NaOH溶液倒吸入Y管中 | ④该反应是气体体积减小的反应,Y管内压强降低,在大气压的作用下发生倒吸 |
6.含有非极性键的离子化合物是( )
| A. | Na2O2 | B. | NaOH | C. | H2 | D. | HC1 |
3.关于生活中的有机物,下列说法正确的是( )
| A. | 所有的糖类、油脂和蛋白质都能发生水解反应 | |
| B. | 工业上利用油脂在碱性条件下的水解反应制取肥皂和甘油 | |
| C. | 做衣服的棉、麻、蚕丝的主要成分都是纤维素 | |
| D. | 人体中没有水解纤维素的酶,所以纤维素在人体中没有任何作用 |
 ②
② ③
③
 依据氧化还原反应:
依据氧化还原反应: