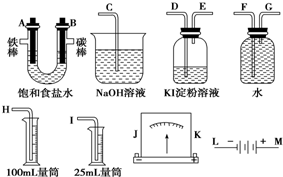
��Ŀ����
16����ʯ���ѻ����ѽ���̵õ�����ϩ����ϩ���ϳɱ�ϩ��������·�����£�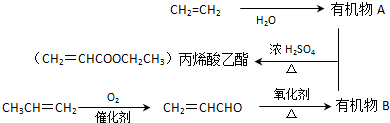
�������ϲ��Ϻ�����ѧ�Ļ�ѧ֪ʶ�ش��������⣺
��1����ϩȩ��CH2=CHCHO���к��еĹ�����̼̼˫����ȩ���������ƣ���
��2��A��B�ϳɱ�ϩ�������Ļ�ѧ����ʽ��CH2=CHCOOH+CH3CH2OH$?_{��}^{Ũ����}$CH2=CHCOOCH2CH3+H2O��
��3����ʯ���ѽ�����ϩ�ϳɾ۱�ϩ���ϵĻ�ѧ����ʽ�ǣ�nCH2=CHCH3$\stackrel{������}{��}$
 ��
��
���� CH2=CH2��ˮ�����ӳɷ�Ӧ������AΪCH3CH2OH��CH2=CHCHO����������Ӧ����BΪCH2=CHCOOH��CH2=CHCOOH��CH3CH2OH����������Ӧ���ɱ�ϩ�����������ݹ����ŵ����ʺͱ仯�жϷ�Ӧ���Ͳ�д����Ӧ�Ļ�ѧ����ʽ��
��� �⣺CH2=CH2��ˮ�����ӳɷ�Ӧ������AΪCH3CH2OH��CH2=CHCHO����������Ӧ����BΪCH2=CHCOOH��CH2=CHCOOH��CH3CH2OH����������Ӧ���ɱ�ϩ��������
��1����ϩȩ��CH2=CHCHO���к��еĹ�������̼̼˫����ȩ�����ʴ�Ϊ��̼̼˫����ȩ����
��2��CH2=CHCOOH��CH3CH2OH����������Ӧ���ɱ�ϩ��������ҲΪȡ����Ӧ����Ӧ�ķ���ʽΪCH2=CHCOOH+CH3CH2OH$?_{��}^{Ũ����}$CH2=CHCOOCH2CH3+H2O��
�ʴ�Ϊ��CH2=CHCOOH+CH3CH2OH$?_{��}^{Ũ����}$CH2=CHCOOCH2CH3+H2O��
��3��CH2=CHCH3����C=C���ɷ����Ӿ۷�Ӧ����Ӧ�ķ���ʽΪnCH2=CHCH3$\stackrel{������}{��}$ ��
��
�ʴ�Ϊ��nCH2=CHCH3$\stackrel{������}{��}$ ��
��
���� ���⿼���л���ĺϳɣ���Ŀ�ѶȲ�����ע����ճ����л���Ĺ����ŵ����ʣ���ס��Ӧ�����������л��ﷴӦ�Ļ�ѧ����ʽҪ��д��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | 11��16 | B�� | 6��8 | C�� | 12��17 | D�� | 20��9 |

| A�� | �ӻ�ȩ�ķ���ʽΪC21H26O | |
| B�� | ά����A���ӽṹ�к��б�����̼̼˫�����ǻ� | |
| C�� | �ӻ�ȩ��ά����A���������� | |
| D�� | 1 mol��1 mol����һ�������¾��������6 mol H2������Ӧ |
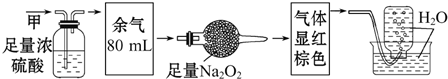
| A�� | NH3��NO2��N2 | B�� | NH3��NO��CO2 | C�� | NH3��NO2��CO2 | D�� | NO��CO2��N2 |
| A�� | CH3Cl | B�� |  | ||
| C�� |  | D�� | 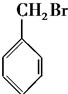 |
| A�� | �ձ����У��������͵�أ�������ӦʽΪ2Al-6e-=2Al3+��������ӦʽΪ 6H++6e-=3H2�� | |
| B�� | �ձ����У������������Һ����Ũ���ᣬ�����͵��ʱ��Ϊ������ͭΪ���� | |
| C�� | �ձ����У�������ͭ�����͵�أ�����Ϊ�������������������͵�أ�����Ϊ���� | |
| D�� | �ձ����У�����������ȫ�ܽ⣬��Һ����ɫ������Һ�еμ�KSCN��Һ����Һ����ɫ |

 ��
��