题目内容
20.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,共转移NA个电子 | |
| B. | 标准状况下,5.6 L一氧化氮和5.6 L氧气混合后的分子总数为0.5NA | |
| C. | 标准状况下,11.2 L HF含有0.5 NA个HF分子 | |
| D. | 500mL 12mol.L-1的盐酸与足量 MnO2加热充分反应,生成Cl2 分子数目1.5 NA |
分析 A.钠与氧气反应无论生成氧化钠还是过氧化钠,钠都变为+1价钠离子;
B.氧气与一氧化氮反应生成二氧化氮,二氧化氮反应生成四氧化二氮;
C.标况下HF为液体;
D.二氧化锰与浓盐酸反应,与稀盐酸不反应.
解答 解:A.钠与氧气反应无论生成氧化钠还是过氧化钠,钠都变为+1价钠离子,1mol钠参加反应生成1mol钠离子转移1mol电子,个数为:NA,故A正确;
B.标准状况下,5.6L(0.25mol)一氧化氮和5.6L(0.25mol)氧气混合后发生反应生成0.25mol的二氧化氮,同时剩余氧气0.125mol,但生成的二氧化氮又能生成四氧化二氮,二者的反应为可逆反应,则分子的总物质的量小于0.375mol,分子数小于0.375NA,故B错误;
C.标况下HF为液体,不能使用气体摩尔体积,故C错误;
D.500mL 12mol.L-1的盐酸与足量 MnO2加热充分反应,随着反应进行,盐酸浓度降低,变为稀盐酸,不与二氧化锰反应,所以生成Cl2 分子数目小于1.5 NA,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的应用,明确气体摩尔体积的使用条件和对象,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系即可解答,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 向KI溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 碘易溶于CCl4,难溶于水 |
| B | 向某溶液中滴加BaCl2溶液,随后加稀硝酸酸化 | 溶液中产生白色沉淀,加稀硝酸不溶解 | 原溶液中一定含有SO42- |
| C | 将稀硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中 | 溶液变黄色 | 氧化性:H2O2比Fe3+强 |
| D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
11.从海带中提取碘,需经过称量、灼烧、溶解、过滤、氧化、萃取和分液等操作,下列图示装置和原理能达到目的是( )
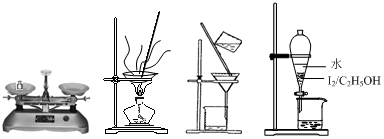

| A. | 称量 | B. | 灼烧 | C. | 过滤 | D. | 萃取 |
15.实验室用氢气还原氧化铜,正确的操作顺序是( )
| A. | 加热、通氢气、停止加热、继续通氢气至试管冷却 | |
| B. | 通氢气、加热、停止加热、继续通氢气至试管冷却 | |
| C. | 通氢气后立即点燃酒精灯加热 | |
| D. | 停止加热后立即停止通氢气 |
5.化学实验设计和操作中必须十分重视安全和环境.下列实验问题处理方法正确的是( )
| A. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| B. | 在气体发生装置上直接点燃一氧化碳气体时,必须要先检验一氧化碳气体的纯度.最简单的方法是用排空气的方法先收集一试管气体,点燃气体,听爆鸣声 | |
| C. | 制氧气时排水法收集氧气后出现倒吸现象,应立即松开试管上的橡皮塞 | |
| D. | 凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |
12.下列说法中正确的是( )
| A. | 氯化钠水溶液在电流的作用下电离出Na+和Cl- | |
| B. | 二氧化碳的水溶液能够导电,故二氧化碳属于电解质 | |
| C. | 硫酸钡难溶于水,但硫酸钡属于电解质 | |
| D. | 氧化钠在水中的电离方程式可表示为Na2O=2Na++O2- |
10.下列有关实验的选项正确的是( )
| A.图装置中X为苯,可用于吸收NH3或HCl,并防止倒吸 | B.图装置可用于铜与浓硫酸反应制取并收集二氧化硫 | C.图装置可用于硫酸铜溶液的蒸发浓缩,然后冷却制硫酸铜晶体 | D.记录滴定终点读数为12.20mL |
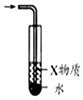 | 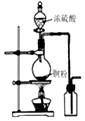 | 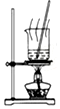 | 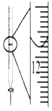 |
| A. | A | B. | B | C. | C | D. | D |
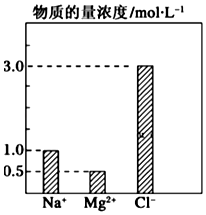 在0.2L由NaCl、MgCl2、BaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
在0.2L由NaCl、MgCl2、BaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题: