题目内容
某学生设计了一个“黑笔写红字”的趣味实验(如图)。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。
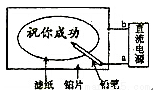
据此,下列叙述正确的是
A.铅笔端作阳极,发生还原反应
B.铂片端作阴极,发生氧化反应
C.铅笔端有少量的氯气产生
D.a点是负极,b点是正极
D
【解析】
试题分析:铅笔芯的主要成分为石墨,石墨是惰性电极,用惰性电极电解氯化钠溶液,阳极反应为2Cl--2e-=Cl2↑,阴极反应为2H2O+2e-=H2↑+2OH-,所以阴极附近变红,故铅笔端作阴极,发生还原反应;铂片端作阳极,发生氧化反应,铂片端有少量氯气生成;a、b点分别是直流电源的负极和正极,选D。
考点:考查电解原理的应用。

练习册系列答案
相关题目
在恒压条件下化学反应:2SO2(g)+O2(g)? ?2SO3(g);ΔH=-Q kJ·mol-1,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列。判断下列叙述正确的是
?2SO3(g);ΔH=-Q kJ·mol-1,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列。判断下列叙述正确的是
容器 | SO2(mol) | O2(mol) | SO3(mol) | N2(mol) | Q(kJ) |
甲 | 2 | 1 | 0 | 0 | Q1 |
乙 | 1 | 0.5 | 0 | 0 | Q2 |
丙 | 0 | 0 | 2 | 0 | Q3 |
丁 | 1 | 0.5 | 0 | 1 | Q4 |
A.平衡时,向甲容器中再加1mol O2,一段时间后达到平衡时O2的体积分数减小
B.平衡时,升高丙容器温度,正反应速率增大,逆反应速率减小,平衡逆向移动
C.各容器中反应放出热量的关系为:Q1=2Q2>2Q4
D.丁容器中反应达到平衡时,其化学平衡常数小于乙容器中反应的平衡常数
 的表述不正确的是
的表述不正确的是 2N2(g)+6H2O(g)在2L的密闭容器中进行,半分钟后N2的物质的量增加了0.6mol。此反应的平均反应速率可表示为
2N2(g)+6H2O(g)在2L的密闭容器中进行,半分钟后N2的物质的量增加了0.6mol。此反应的平均反应速率可表示为 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2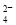 +H+=BaSO4↓+H2O
+H+=BaSO4↓+H2O



