题目内容
(11分)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
(1)冶炼铜的反应为:8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
(2)上述冶炼过程产生大量SO2。下列处理方案中合理的是 (填代号)。
a.高空排放 b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO4 d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I—氧化为I2:S2O82—+2I—=2SO42—+I2。通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应催化的过程: 、 (不必配平)
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为:
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
a.除去Al3+的离子方程式是 。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为 。
证明炉渣中含有FeO的实验现象为 。
(1)Cu、O;(2分)
(2)b、c;(2分,各1分)
(3)2Fe3++2I—=2Fe2++I2;(1分)S2O82—+2Fe2+=2SO42—+2Fe3+;(1分)
(离子方程式不配平不扣分,顺序颠倒不扣分)
(4)a:2Al3++4OH—=AlO2—+2H2O[或Al3++4OH—=Al(OH)4—];(1分)
b:稀硫酸、KMnO4溶液;(2分,各1分)
稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色。(2分)
【解析】
试题分析:(1)反应8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2中铜元素的化合价由+2价降为0价,氧元素的化合价由0价降为—2价,被还原的元素是Cu、O;(2)冶炼过程产生大量SO2.分析下列处理方案:a.二氧化硫是污染性气体,高空排放会污染空气,处理不合理;b.可以利用吸收二氧化硫生成硫酸,合理;c.用纯碱溶液吸收二氧化硫可以制Na2SO4,合理;d.用浓硫酸不能吸收二氧化硫,不合理;答案为:b、c;(3)三价铁具有氧化性,能将碘离子氧化,S2O82-能将亚铁离子氧化,原理为:2Fe3++2I-=2Fe2++I2,S2O82-+2Fe2+=2SO42-+2Fe3+;(4)a.氧化铝是两性氧化物,能和强酸以及强碱反应,6H++AI2O3=3H2O+2Al3+,除去铝离子的反应是利用过量氢氧化钠溶液和铝离子反应生成四羟基合铝,答案为:Al3++4OH-=2H2O+AlO2-;b.高锰酸钾溶液能氧化亚铁离子,使得高锰酸钾溶液褪色,答案为:稀硫酸、KMnO4溶液;稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色。
8Cu+4FeO+2Fe2O3+16SO2中铜元素的化合价由+2价降为0价,氧元素的化合价由0价降为—2价,被还原的元素是Cu、O;(2)冶炼过程产生大量SO2.分析下列处理方案:a.二氧化硫是污染性气体,高空排放会污染空气,处理不合理;b.可以利用吸收二氧化硫生成硫酸,合理;c.用纯碱溶液吸收二氧化硫可以制Na2SO4,合理;d.用浓硫酸不能吸收二氧化硫,不合理;答案为:b、c;(3)三价铁具有氧化性,能将碘离子氧化,S2O82-能将亚铁离子氧化,原理为:2Fe3++2I-=2Fe2++I2,S2O82-+2Fe2+=2SO42-+2Fe3+;(4)a.氧化铝是两性氧化物,能和强酸以及强碱反应,6H++AI2O3=3H2O+2Al3+,除去铝离子的反应是利用过量氢氧化钠溶液和铝离子反应生成四羟基合铝,答案为:Al3++4OH-=2H2O+AlO2-;b.高锰酸钾溶液能氧化亚铁离子,使得高锰酸钾溶液褪色,答案为:稀硫酸、KMnO4溶液;稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色。
考点:考查氧化还原反应基本概念、离子方程式的书写、离子检验的实验设计。

下列实验方案中,不能达到实验目的是
选项 | 实验目的 | 实验方案 |
A | 验证Ksp(AgCl)>Ksp(AgI) | 向NaCl溶液中滴加AgNO3溶液,产生白色沉淀,再滴加KI溶液,可观察到白色沉淀转化为黄色沉淀 |
B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置。可观察到下层液体呈紫色 |
D | 比较确定铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液 |
 2Z影响的示意图。下列叙述正确的是
2Z影响的示意图。下列叙述正确的是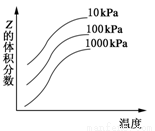
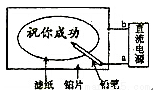
 Y的说法错误的是
Y的说法错误的是 Y 是两种不同的核素
Y 是两种不同的核素