题目内容
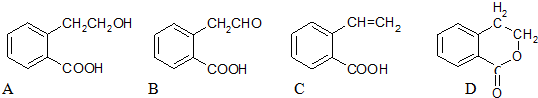
19.有机物A是合成高分子树脂(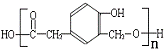 )和某合成鞣剂(
)和某合成鞣剂( 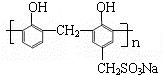 )
)的原料之一.相关的合成路线如下图所示(某些生成物已略去):
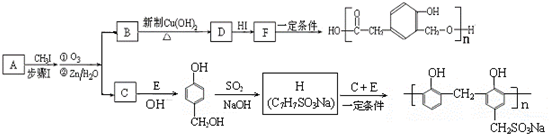
已知:Ⅰ.
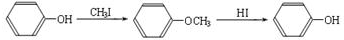
Ⅱ.
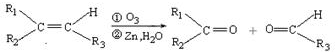 (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)请回答下列问题:
(1)经质谱测定,有机物A的相对分子质量为164,燃烧8.2 g有机物A,生成标准状况下11.2 L CO2和5.4 g H2O.则A的分子式是C10H12O2.
(2)步骤Ⅰ的目的是保护酚羟基;
(3)将有机物E溶液滴到饱和溴水中,有大量白色沉淀生成.E的含氧官能团的名称是羟基.H→合成鞣剂的反应类型是缩聚反应.
(4)B→D的化学方程式是
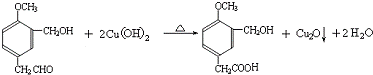 .
.(5)F→高分子树脂的化学方程式是
 .
.(6)F的同分异构体X具有如下特点:①与F具有相同的官能团;②苯环上有两个取代基;③1 mol X 最多消耗Na、NaOH、NaHCO3 的物质的量分别为3、2、1.且X有如下转化关系:

香豆素的结构简式为
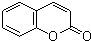 ,写出 X可能的结构简式为
,写出 X可能的结构简式为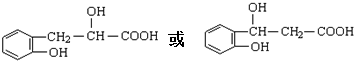 .
.
分析 有机物A的相对分子质量为164,8.2g有机物A的物质的量=$\frac{8.2g}{164g/mol}$=0.05mol,完全燃烧生成标准状况下11.2LCO2和5.4gH2O,则二氧化碳为$\frac{11.2L}{22.4L/mol}$=0.5mol,水为$\frac{5.4g}{18g/mol}$=0.3mol,则有机物A中N(C)=$\frac{0.5mol}{0.05mol}$=10、N(H)=$\frac{0.3mol×2}{0.05mol}$=12,则N(O)=$\frac{164-10×12-12}{16}$=2,故则A的分子式是C10H12O2.
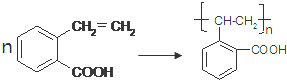
F在一定条件下合成高分子树脂( ),应是发生酯化反应,故F为
),应是发生酯化反应,故F为 ,A发生信息反应生成B、C,B能被新制氢氧化铜氧化生成D,则B含有-CHO、D含有-COOH,D发生信息Ⅱ中第二步反应生成F,则D含有-OCH3,结合F的结构可知,D为
,A发生信息反应生成B、C,B能被新制氢氧化铜氧化生成D,则B含有-CHO、D含有-COOH,D发生信息Ⅱ中第二步反应生成F,则D含有-OCH3,结合F的结构可知,D为 ,则B为
,则B为 .有机物E溶液滴到饱和溴水中,有大量白色沉淀生成,则E含有酚羟基,结合C与E反应产物结构、H与C、E反应产物结构可知,C为HCHO、E为
.有机物E溶液滴到饱和溴水中,有大量白色沉淀生成,则E含有酚羟基,结合C与E反应产物结构、H与C、E反应产物结构可知,C为HCHO、E为 ,综上所述,A的结构为
,综上所述,A的结构为 ,据此解答.
,据此解答.
解答 解:有机物A的相对分子质量为164,8.2g有机物A的物质的量=$\frac{8.2g}{164g/mol}$=0.05mol,完全燃烧生成标准状况下11.2LCO2和5.4gH2O,则二氧化碳为$\frac{11.2L}{22.4L/mol}$=0.5mol,水为$\frac{5.4g}{18g/mol}$=0.3mol,则有机物A中N(C)=$\frac{0.5mol}{0.05mol}$=10、N(H)=$\frac{0.3mol×2}{0.05mol}$=12,则N(O)=$\frac{164-10×12-12}{16}$=2,故则A的分子式是C10H12O2.
F在一定条件下合成高分子树脂( ),应是发生酯化反应,故F为
),应是发生酯化反应,故F为 ,A发生信息反应生成B、C,B能被新制氢氧化铜氧化生成D,则B含有-CHO、D含有-COOH,D发生信息Ⅱ中第二步反应生成F,则D含有-OCH3,结合F的结构可知,D为
,A发生信息反应生成B、C,B能被新制氢氧化铜氧化生成D,则B含有-CHO、D含有-COOH,D发生信息Ⅱ中第二步反应生成F,则D含有-OCH3,结合F的结构可知,D为 ,则B为
,则B为 .有机物E溶液滴到饱和溴水中,有大量白色沉淀生成,则E含有酚羟基,结合C与E反应产物结构、H与C、E反应产物结构可知,C为HCHO、E为
.有机物E溶液滴到饱和溴水中,有大量白色沉淀生成,则E含有酚羟基,结合C与E反应产物结构、H与C、E反应产物结构可知,C为HCHO、E为 ,综上所述,A的结构为
,综上所述,A的结构为 ,
,
(1)由上述分析可知,A的分子式为:C10H12O2,故答案为:C10H12O2;
(2)反应中将醛基氧化为羧基,也可以氧化酚羟基,反应开始酚羟基发生反应,将醛基氧化为羧基后,D到F又产生酚羟基,故步骤Ⅰ的目的是保护酚羟基,
故答案为:保护酚羟基;
(3)E是苯酚,含氧官能团的名称是羟基,由物质结构可知,H→合成鞣剂的反应中除生成高聚物外,还原小分子物质生成,属于缩聚反应,
故答案为:羟基;缩聚反应;
(4)B→D的化学方程式是 ,
,
故答案为: ;
;
(5)F→高分子树脂的化学方程式是 ,
,
故答案为: ;
;
(6)F的同分异构体X具有如下特点:与F具有相同的官能团,1mol X 最多消耗Na、NaOH、NaHCO3的物质的量分别为3、2、1,则X中含有1个-COOH、1个酚羟基、1个醇羟基,苯环上有两个取代基,则侧链为-OH、-CH2CH(OH)COOH或-CH(OH)CH2COOH,结合香豆素的结构简式 ,可知X中两个取代基处于邻位位置,故X的结构简式为
,可知X中两个取代基处于邻位位置,故X的结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物的推断与合成,侧重考查学生分析推断及获取信息解答问题能力,需要学生对给予的信息进行利用,为高频考点,注意根据有机物的结构结合反应信息通过顺推法与逆推法相结合进行推断,知道常见有机物结构和性质,题目难度不大.

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案| A. | NH4+、Fe2+、Cl-、SO42- | B. | Na+、K+、Cl-、SO42- | ||
| C. | Mg2+、AlO2-、Cl-、SO42- | D. | K+、Ca2+、HCO3-、Cl- |
| CO2(g) | H2(g) | CO(g) | H2O(g) | |
| 甲 | a mol | a mol | 0 | 0 |
| 乙 | a mol | 2a mol | 0 | 0 |
| 丙 | a mol | a mol | 0 | a mol |
| 丁 | amol | amol | amol | amol |
| A. | n(丁)>n(甲)>n(乙)>n(丙) | B. | n(丁)>n(甲)>n(丙)>n(乙) | C. | n(丁)>n(乙)>n(丙)>n(甲) | D. | n(丁)>n(乙)>n(甲)>n(丙) |
| A. | 除去混在NO2中的NO:将气体与足量O2混合 | |
| B. | 除去混在CO2中的SO2:将气体依次通过足量酸性KMnO4溶液和浓硫酸 | |
| C. | 除去KCl溶液中的K2CO3:加入过量BaCl2溶液后过滤 | |
| D. | 除去乙酸中混有的乙醇:加入金属钠后蒸馏 |
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |

Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入0.1mol苯甲酸和0.4mol 甲醇,再小心加入 3mL浓硫酸,混匀后,投入几粒沸石,小心加热使反应完全,得苯甲酸甲酯粗产品.
(1)甲装置的作用是:冷凝回流;冷却水从b(填“a”或“b”)口进入.
(2)化学小组在实验中用过量的反应物甲醇,其理由是该合成反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,增加甲醇投料量提高产率或苯甲酸的转化率.
Ⅱ.粗产品的精制
苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用如图2流程进行精制.
(3)试剂1可以是B(填编号),作用是洗去苯甲酸甲酯中过量的酸;
A.稀硫酸 B.碳酸钠溶液 C.乙醇
(4)操作2中,收集产品时,控制的温度应在199.6℃;
(5)实验制得的苯甲酸甲酯精品质量为10g,则苯甲酸的转化率为73.5%;
(6)本实验制得的苯甲酸甲酯的产量低于理论产量,可能的原因是C(填编号).
A.蒸馏时从100℃开始收集产品 B.甲醇用量多了 C.制备粗品时苯甲酸被蒸出.
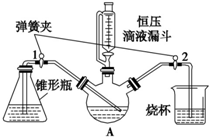 某化学兴趣小组用下图实验装置进行醋酸亚铬的制备研究.已知:醋酸亚铬(其中铬元素为二价)是红棕色晶体,不溶于水,在潮湿时,Cr2+极易被氧化成 Cr3+.(备注:Cr2+在溶液中为蓝色).
某化学兴趣小组用下图实验装置进行醋酸亚铬的制备研究.已知:醋酸亚铬(其中铬元素为二价)是红棕色晶体,不溶于水,在潮湿时,Cr2+极易被氧化成 Cr3+.(备注:Cr2+在溶液中为蓝色).

 .
.
 如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.打开活塞,使NO与O2充分反应(2NO+O2=2NO2).(不考虑NO2与N2O4的转化)
如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.打开活塞,使NO与O2充分反应(2NO+O2=2NO2).(不考虑NO2与N2O4的转化)