题目内容
17.如图所示的钢铁腐蚀中,下列说法正确的是( )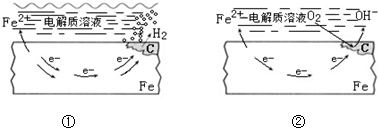
| A. | ①、②中的Fe都发生的是还原反应 | |
| B. | ①表面的电解质溶液可以为NaCl溶液 | |
| C. | 生活中钢铁制品的腐蚀以图①所示为主 | |
| D. | 图②中,正极反应式为O2+4e-+2H2O═4OH- |
分析 根据图知,①为铁的析氢腐蚀,②为铁的吸氧腐蚀,酸性条件下钢铁发生消去反应,弱酸性或中性条件下钢铁发生吸氧腐蚀,在生活中钢铁主要以吸氧腐蚀为主,钢铁被腐蚀的最终产物是Fe2O3.xH2O,发生吸氧腐蚀时正极上氧气得电子发生还原反应.
解答 解:根据图知,①为铁的析氢腐蚀,②为铁的吸氧腐蚀,
A.①②铁的腐蚀装置中,都是金属Fe易失电子作负极、发生氧化反应,故A错误;
B.根据图知,①为铁的析氢腐蚀,电解质是酸性的溶液,不是中性,故B错误;
C.生活中钢铁主要以吸氧腐蚀为主,以图②所示为主,故C错误;
D.图②中铁发生吸氧腐蚀,正极反应式为O2+4e-+2H2O═4OH-,故D正确;
故选D.
点评 本题考查金属的腐蚀与防护,明确钢铁发生析氢腐蚀和吸氧腐蚀的条件是解本题关键,知道各个电极上发生的反应,会正确书写电极反应式,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.乙醇是重要的有机化工原料,可由乙烯直接水合法或间接水合法生产.回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H).再水解生成乙醇.写出相应的反应的化学方程式C2H4+H2SO4=C2H5OSO3H、C2H5OSO3H+H2O→C2H5OH+H2SO4.
(2)已知:乙烯气相直接水合反应如下:
C2H4(g)+H2O(g)?C2H5OH(g) H=-45.5KJ/mol
下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中n(H2O):n(C2H4)=1:1)

①计算乙烯水合制乙醇反应在图中A点的平衡常数Kp=0.07(MPa)-1(Kp表示用平衡分压代替平衡浓度计算出的平衡常数的值,分压=总压×物质的量分数)
②图中压强P1、P2、P3、P4的大小顺序为:p1<p2<p3<p4,理由是反应分子数减少,相同温度下,压强升高乙烯转化率提高.
(3)若某温度下,反应C2H4(g)+H2O(g)?C2H5OH(g)的平衡常数为Kp=0.05MPa-1,体系总压为8.00MPa,各物质的量分数如下表所示.
则v(正)<v(逆)(填“>”“<”“=”).
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H).再水解生成乙醇.写出相应的反应的化学方程式C2H4+H2SO4=C2H5OSO3H、C2H5OSO3H+H2O→C2H5OH+H2SO4.
(2)已知:乙烯气相直接水合反应如下:
C2H4(g)+H2O(g)?C2H5OH(g) H=-45.5KJ/mol
下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中n(H2O):n(C2H4)=1:1)

①计算乙烯水合制乙醇反应在图中A点的平衡常数Kp=0.07(MPa)-1(Kp表示用平衡分压代替平衡浓度计算出的平衡常数的值,分压=总压×物质的量分数)
②图中压强P1、P2、P3、P4的大小顺序为:p1<p2<p3<p4,理由是反应分子数减少,相同温度下,压强升高乙烯转化率提高.
(3)若某温度下,反应C2H4(g)+H2O(g)?C2H5OH(g)的平衡常数为Kp=0.05MPa-1,体系总压为8.00MPa,各物质的量分数如下表所示.
| 物质 | C2H4(g) | H2O(g) | C2H5OH(g) |
| 物质的量分数 | 0.25 | 0.25 | 0.5 |
5.下列反应的离子方程式书写正确的是( )
| A. | 硫酸铝溶液中加入过量氨水:Al3++3OH-═Al(OH)3↓ | |
| B. | 在氢氧化钡溶液中逐滴加入硫酸氢钠溶液至恰好呈中性:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| C. | 硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H-+H2O2═Fe3++2H2O | |
| D. | 碳酸钙与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O |
12.某烃的结构简式为 ,它可能具有的性质是( )
,它可能具有的性质是( )
 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 易溶于水,也易溶于有机溶剂 | |
| B. | 1 mol该烃含有4 mol碳碳双键 | |
| C. | 能发生聚合反应,其产物可表示为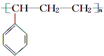 | |
| D. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色 |
2.下列说法或表示方法不正确的是( )
| A. | 盖斯定律实质上是能量守恒定律的体现 | |
| B. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多 | |
| C. | 由C(石墨)→C(金刚石);△H=+73 kJ/mol,可知石墨比金刚石稳定 | |
| D. | 在稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ |
9.可以用浓磷酸代替浓硫酸制取溴化氢气体的理由是( )
| A. | 浓磷酸与浓硫酸的性质相似 | |
| B. | 浓磷酸与浓硫酸一样难挥发,且属非氧化性酸 | |
| C. | 浓磷酸无氧化性,只有还原性 | |
| D. | 浓磷酸的酸性强于氢溴酸 |
7.下列溶液中有关微粒的物质的量浓度关系错误的是( )
| A. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(NH4+)+c(OH-)>c(Cl-)+c(H+) | |
| B. | 等体积、等物质的量浓度为Na2CO3溶液与NaHCO3溶液混合后:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) | |
| C. | 浓度相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液中,c(NH4+)大小顺序为:②>③>① | |
| D. | 0.1 mol/L Na2CO3溶液与0.1 mol/L HCl溶液等体积混合,所得溶液中:c(H+)+c(H2CO3)=c(CO32-)+c(OH-) |
