题目内容
4. 我国在青藏高原发现了名为“可燃冰”的环保型新能源.?
我国在青藏高原发现了名为“可燃冰”的环保型新能源.?(1)CH4可与Cl2反应,反应历程如图?
①Cl2→2Cl•△H=243kJ•mol-1
②Cl•+CH4→•CH3+HCl△H=4kJ•mol-1
③•CH3+Cl2→CH3Cl+Cl•△H=-106kJ•mol-1
则CH4与Cl2反应生成CH3Cl(g)的热化学方程式为CH4(g)+Cl2(g)→CH3Cl(g)+HCl(g)△H=-102kJ•mol-1.
(2)CH4可用于设计燃料电池,甲烷燃料电池的工作原理如右图所示:
则通入CH4的一极为原电池的负极(填“正极”或“负极”),负极的电极反应式为CH4-8e-+10OH-=CO32-+7H2O.
分析 (1)①Cl-Cl→2Cl△H=243kJ•mol-1
②Cl•+CH3-H→CH3+H-Cl△H=4kJ•mol-1
③•CH3+Cl-Cl→CH3--Cl+Cl•△H=-106kJ•mol-1 ;
依据盖斯定律②+③计算得到;
(2)燃料电池中燃料在负极失电子发生氧化反应,正极是氧气得到电子发生还原反应.
解答 解:(1)①Cl-Cl→2Cl△H=243kJ•mol-1
②Cl•+CH3-H→CH3+H-Cl△H=4kJ•mol-1
③•CH3+Cl-Cl→CH3-Cl+Cl•△H=-106kJ•mol-1 ;
依据盖斯定律②+③得到:CH4(g)+Cl2(g)→CH3Cl(g)+HCl(g)△H=-102 kJ•mol-1;
故答案为:CH4(g)+Cl2(g)→CH3Cl(g)+HCl(g)△H=-102 kJ•mol-1;
(2)甲烷燃料电池,燃料电池中燃料甲烷在负极失电子发生氧化反应,电解质溶液是氢氧化钾溶液,负极电极反应为:CH4-8e-+10OH-=CO32-+7H2O;
故答案为:负极; CH4-8e-+10OH-=CO32-+7H2O.
点评 本题考查了热化学方程式和盖斯定律的应用,原电池的电极反应分析,注意燃料电池电解质溶液的酸碱性,题目难度中等.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
15.测定硫酸铜晶体中结晶水含量时,要用到下列仪器中的( )
| A. |  | B. |  | C. |  | D. |  |
12.在一定条件下,2SO2(g)+O2(g)?2SO3(g)+Q(Q>0)反应已达到平衡,若保持其他条件不变,升高反应体系温度,则下列说法错误的是( )
| A. | 正、逆反应速率都增大 | B. | 正反应速率减小,逆反应速率增大 | ||
| C. | 平衡向逆反应方向移动 | D. | 混合气体中SO2的体积百分数增大 |
13.KW仅仅是温度的函数.下列关于KW与温度关系的叙述中,正确的是( )
| A. | 温度越高,KW越大 | |
| B. | 温度越低,KW越大 | |
| C. | 随着温度的升高,KW可能增大也可能减小 | |
| D. | 随着温度的升高,KW肯定增大,H+和OH-浓度同时升高 |

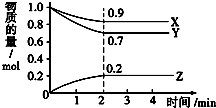 某温度时,在2L密闭容器中,X、Y、Z三种气体物质的物质的量随时间变化的曲线如图所示,由图中数据分析:
某温度时,在2L密闭容器中,X、Y、Z三种气体物质的物质的量随时间变化的曲线如图所示,由图中数据分析: