��Ŀ����
9��SO3�ǹ�ҵ����Ҫ���м��壬�ӽṹ��ȥ�о�����ʶ�����б�Ҫ����֪SO3�е� �塢���������ά״���ӣ���1��SO3��S���ӻ��������Ϊsp2��������Ԫ��λ��Ԫ�����ڱ��еڶ����ڢ�A�壮
��2�������壨SO3��3����ά״��SO3��n�Ĺ�ϵΪD������ĸ����
A��ͬϵ�� B��ͬ���칹��C��ͬ��������D������Ԫ��������ͬ
��3����Һ̬ʱ����������壨SO3��3����ƽ��״̬���¶�Խ�ߣ������壨����塱�������塱��Խ�٣�
��4��SO3�����ڹ�ҵ�������ᣬ����������ɫ��״��Һ�壬�ȽϺã���ԭ����������Ӽ���������
���� ��1��SO3��S�γ�3���Ҽ����µ��Ӷ���Ϊ$\frac{6-2��3}{2}$=0���Դ��жϣ�
��2�������壨SO3��3����ά״��SO3��n��Ϊ�������������ͬ��Ԫ�أ�
��3����������������ķ�ӦΪ���Ϸ�Ӧ����Ӧ�ų�������
��4��������Ӽ���������
��� �⣺��1��SO3��S�γ�3���Ҽ����µ��Ӷ���Ϊ$\frac{6-2��3}{2}$=0���۲���Ӷ���Ϊ3��Ϊsp2�ӻ�����Ԫ��λ��Ԫ�����ڱ��еڶ����ڢ�A�壬
�ʴ�Ϊ��sp2�� ������A��
��2�������壨SO3��3����ά״��SO3��n��Ϊ�����������ͬϵ�ͬ���칹�壬Ҳ����ͬ�������壬������ͬ��Ԫ�أ��ʴ�Ϊ��D��
��3����������������ķ�ӦΪ���Ϸ�Ӧ����Ӧ�ų��������������¶�ƽ�������ƶ�����������٣��ʴ�Ϊ�������壻
��4������O�ķǽ����Խ�ǿ����Ӧ���⻯����Ӽ��������������к���O-H�������γ�������е�ϸߣ��ʴ�Ϊ��������Ӽ���������
���� ���⿼�����ʵĽṹ�����ʣ�Ϊ��Ƶ���㣬���ؿ���ѧ���ķ�����������Ҫ�������ʵĽṹ�ص��Լ���ظ�������⣬�ѶȲ���

��ϰ��ϵ�д�
 A�ӽ��� ϵ�д�
A�ӽ��� ϵ�д� ȫ�Ų��Ծ�ϵ�д�
ȫ�Ų��Ծ�ϵ�д�
�����Ŀ
3������ָ����Ӧ�����ӷ���ʽ��ȷ���ǣ�������
| A�� | ����ˮ��Ӧ��Na+2H2O�TNa++2OH-+H2�� | |
| B�� | ��ⱥ��ʳ��ˮ��ȡ�ռ��������2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$H2��+Cl2��+2OH- | |
| C�� | ������������Һ�м���ϡ���Ba2++OH-+H++SO42-�TBaSO4��+H2O | |
| D�� | ��̼�������Һ�м�������ʯ��ˮ��Ca2++HCO3-+OH-�TCaCO3��+H2O |
4��W��R��X��Y��Z��ԭ��������������Ķ���������Ԫ�أ�Yԭ�Ӱ뾶�ڶ���������Ԫ�������W��Yͬ���壬X��Zͬ���壮Rԭ���������������ڲ��������3��W��Yԭ�ӵĵ������ܺ���X��Zԭ�ӵĵ������ܺ�֮��Ϊ1��2������˵����ȷ���ǣ�������
| A�� | ԭ�Ӱ뾶��r��X����r��R����r��W�� | |
| B�� | X��Yֻ���γ�һ�ֻ����� | |
| C�� | X�ļ���̬�⻯������ȶ��Ա�Z���� | |
| D�� | ��W��R��X����Ԫ����ɵĻ�����������ᡢ����� |
14����֪��W�������Ϣ���ٹ�·�Ǽܵ�Ԫ��֮һ����X��Y��Z��W��Ԫ�����ڱ��е�λ����ͼ��ʾ������˵����ȷ���ǣ�������
| X | Y | |
| Z | W |
| A�� | ��������ϼۣ�X=W��Y��Z | |
| B�� | ԭ�Ӱ뾶��W��Z��Y��X | |
| C�� | ����������Ӧˮ��������ԣ�Z��X��W��Y | |
| D�� | ��ۺ������������Һ����SO2��Ӧ�ģ�X��Y��Z��W |
1��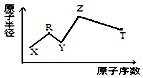 ���ж���������Ԫ��X��Y��Z��R��T��Rԭ�������������ǵ��Ӳ�����2����Y��Z���γ�Z2Y��Z2Y2�����ӻ����Z��T�γɵ�Z2T ���������ƻ�ˮ�ĵ���ƽ�⣬����Ԫ�ص�ԭ�Ӱ뾶��ԭ�������Ĺ�ϵ��ͼ��ʾ�������ƶ���ȷ���ǣ�������
���ж���������Ԫ��X��Y��Z��R��T��Rԭ�������������ǵ��Ӳ�����2����Y��Z���γ�Z2Y��Z2Y2�����ӻ����Z��T�γɵ�Z2T ���������ƻ�ˮ�ĵ���ƽ�⣬����Ԫ�ص�ԭ�Ӱ뾶��ԭ�������Ĺ�ϵ��ͼ��ʾ�������ƶ���ȷ���ǣ�������
 ���ж���������Ԫ��X��Y��Z��R��T��Rԭ�������������ǵ��Ӳ�����2����Y��Z���γ�Z2Y��Z2Y2�����ӻ����Z��T�γɵ�Z2T ���������ƻ�ˮ�ĵ���ƽ�⣬����Ԫ�ص�ԭ�Ӱ뾶��ԭ�������Ĺ�ϵ��ͼ��ʾ�������ƶ���ȷ���ǣ�������
���ж���������Ԫ��X��Y��Z��R��T��Rԭ�������������ǵ��Ӳ�����2����Y��Z���γ�Z2Y��Z2Y2�����ӻ����Z��T�γɵ�Z2T ���������ƻ�ˮ�ĵ���ƽ�⣬����Ԫ�ص�ԭ�Ӱ뾶��ԭ�������Ĺ�ϵ��ͼ��ʾ�������ƶ���ȷ���ǣ�������| A�� | ԭ�Ӱ뾶�����Ӱ뾶�����㣺Y��Z | |
| B�� | Y�ĵ�������R��T���⻯�ﷴӦ | |
| C�� | ����������Ӧ��ˮ��������ԣ�T��R | |
| D�� | ��X��R��Y��Z����Ԫ����ɵĻ�����ˮ��Һһ���Լ��� |
18������CO2���ŷ��Լ�CO2����Դ�����þ�����Ҫ���壮
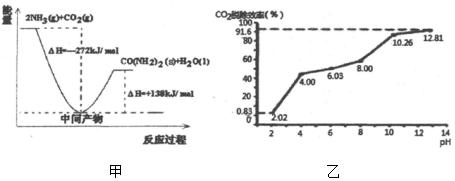
��1��H2NCOONH4�ǹ�ҵ�ϳ�����[CO��NH2��2]���м����÷�Ӧ�������仯ʾ��ͼ��ͼ����ʾ����CO2�Ͱ����ϳ����ص��Ȼ�ѧ����ʽΪCO2��g��+2NH3��g��=CO��NH2��2��s��+H2O��l����H=-134kJ/mol��
��2���ð�ˮ���������е�CO2������Σ��Ǽ���CO2�ŷŵĿ��д�ʩ֮һ��
��д����ˮ���������е�CO2����̼����淋���Ҫ��ѧ����ʽCO2+NH3��H2O=NH4HCO3��
�ڷֱ��ò�ͬpH�����ռ����������е�CO2��CO2�ѳ�Ч�������ռ���pH��ϵ��ͼ����ʾ��������CO2�ĺ���Ϊ12%������ͨ�백ˮ������Ϊ0.052m3/h����״��������pHΪ12.81�İ�ˮ��������30min���ѳ���CO2�����ʵ������Ϊ0.13mol����ȷ��0.01����
��ͨ��������¶����ߣ�CO2�ѳ�Ч����ߣ�������40��ʱ���ѳ�CO2Ч�ʽ��͵���Ҫԭ����̼����������ֽ�����CO2��
��3����CO2�ͼ��������ƺϳ�����CO��H2����CO2��Դ�����õ���Ч;�����ϳ��������Ʊ��״��ķ�ӦΪ2H2��g��+CO��g��?CH3OH��g����H=-90kJ/mol����T1��ʱ���ݻ���ͬ�ļס��ҡ������������ܱ������У�����ͬ��ʽͶ�뷴Ӧ���÷�Ӧ��������ͼ��ʾ��
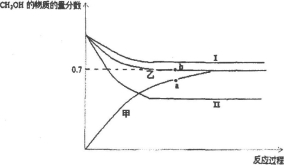
���ܴ�������Ӧ��������I��ѡ��I��II����a��b���ѹǿ��ϵΪPa��Pb���������=����������ƽ��ʱa��״������ʵ�������С���������ʵ�����
��b��ʱ��Ӧ���յ�����Ϊ11.25kJ��

��1��H2NCOONH4�ǹ�ҵ�ϳ�����[CO��NH2��2]���м����÷�Ӧ�������仯ʾ��ͼ��ͼ����ʾ����CO2�Ͱ����ϳ����ص��Ȼ�ѧ����ʽΪCO2��g��+2NH3��g��=CO��NH2��2��s��+H2O��l����H=-134kJ/mol��
��2���ð�ˮ���������е�CO2������Σ��Ǽ���CO2�ŷŵĿ��д�ʩ֮һ��
��д����ˮ���������е�CO2����̼����淋���Ҫ��ѧ����ʽCO2+NH3��H2O=NH4HCO3��
�ڷֱ��ò�ͬpH�����ռ����������е�CO2��CO2�ѳ�Ч�������ռ���pH��ϵ��ͼ����ʾ��������CO2�ĺ���Ϊ12%������ͨ�백ˮ������Ϊ0.052m3/h����״��������pHΪ12.81�İ�ˮ��������30min���ѳ���CO2�����ʵ������Ϊ0.13mol����ȷ��0.01����
��ͨ��������¶����ߣ�CO2�ѳ�Ч����ߣ�������40��ʱ���ѳ�CO2Ч�ʽ��͵���Ҫԭ����̼����������ֽ�����CO2��
��3����CO2�ͼ��������ƺϳ�����CO��H2����CO2��Դ�����õ���Ч;�����ϳ��������Ʊ��״��ķ�ӦΪ2H2��g��+CO��g��?CH3OH��g����H=-90kJ/mol����T1��ʱ���ݻ���ͬ�ļס��ҡ������������ܱ������У�����ͬ��ʽͶ�뷴Ӧ���÷�Ӧ��������ͼ��ʾ��

| ���� | �� | �� | �� |
| ��ʼ��Ӧ��Ͷ���� | 2molH2��1molCO | 1molCH3OH | 2mol CH3OH |
��b��ʱ��Ӧ���յ�����Ϊ11.25kJ��
7�����������У����ڹ��ۻ�������ǣ�������
| A�� | Na2S | B�� | NH4NO3 | C�� | H2 | D�� | CS2 |
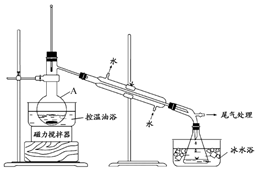 1-�������һ����Ҫ���л��ϳ��м��壬�е�Ϊ71�棬�ܶ�Ϊ1.36g•cm-3��ʵ�����Ʊ�����1-��������Ҫ�������£�
1-�������һ����Ҫ���л��ϳ��м��壬�е�Ϊ71�棬�ܶ�Ϊ1.36g•cm-3��ʵ�����Ʊ�����1-��������Ҫ�������£�