��Ŀ����
17��CH4��H2��C�������ʵ���Դ���ʣ�����ȼ�յ��Ȼ�ѧ����ʽΪ����CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-890.3kJ/mol
��2H2��g��+O2��g���T2H2O��l����H=-571.6kJ/mol
��C��s��+O2��g���TCO2��g����H=-393.5kJ/mol
��1����д���һ�ּ���ϸ������������øʹ������O2���ò���������������ϸ��ʹ1mol��������CO2������Һ̬ˮ���ų�������=���������������=����890.3kJ��
��2��������CO2�����ںϳɺϳ�������Ҫ�ɷ���һ����̼����������CH4+CO2�T2CO+2H2��1gCH4��ȫ��Ӧ���ͷ�15.46kJ����������
��ͼ1���ܱ�ʾ�÷�Ӧ�����������仯����D������ĸ����
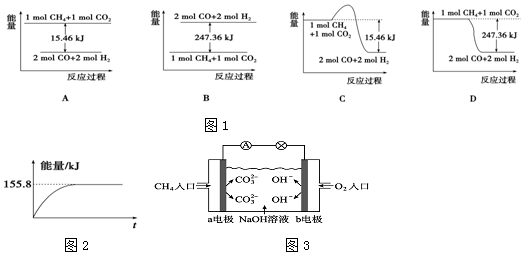
���������ʵ�����Ϊ1mol��CH4��CO2����ij�����ܱ������У���ϵ�ų�����������ʱ��ı仯��ͼ2��ʾ����CH4��ת����ԼΪ63%��
��3��C��s����H2��g������Ӧ������C��s��+2H2��g���TCH4��g���ķ�Ӧ����ֱ�Ӳ�������ͨ��������Ӧ�����C��s��+2H2��g���TCH4��g���ķ�Ӧ�ȡ�H=-74.8kJ•mol-1 ��
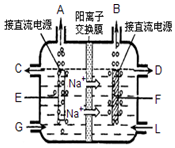
��4��ͼ3�Ǽ���ȼ�ϵ��ԭ��ʾ��ͼ����ش��������⣺
�ٵ�صĸ�����a���a����b�����缫�������ϵĵ缫��Ӧ��O2+2H2O+4e-=4OH-����
�ڵ�ع���һ��ʱ���������Һ��pH��С���������С�����䡱����
���� ��1��CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-890��.3kJ•mol-1���õ�����ϸ��ʹ1mol��������CO2������Һ̬ˮ�ų���������
��2���ټ�����CO2�����ںϳɺϳ�������Ҫ�ɷ���һ����̼����������CH4+CO2�T2CO+2H2��1g CH4��ȫ��Ӧ���ͷ�15.46kJ������������1mol������ȫ��Ӧ�ų�����������ӦΪ���ȷ�Ӧ���ݴ˷���ͼ���жϣ�
�����ݢټ���õ��ķ�Ӧ���ʱ䣬ͼ���Ƿ�Ӧ�ﵽƽ��״̬ʱ����155.8KJ�����㷴Ӧ�ļ���õ�ת���ʣ�
��3����֪����CH4��g��+2O2��g��=CO2��g��+2H2O��l������H1=-890.3kJ/mol��
��2H2��g��+O2��g���T2H2O��l����H=-571.6kJ•mol-1
��C��s��+O2��g��=CO2��g������H2=-393.5kJ/mol
��ӦC��ʯī��s��+2H2��g��=CH4��g�������Ǣ�+��-�ٵõ����ɴ˷������
��4���ټ��Լ���ȼ�ϵ����ͨ������һ��Ϊԭ��صĸ�����ͨ��������һ��Ϊԭ��ص���������������ȼ�Ϸ���ʧ���ӵ�������Ӧ��
�ڸ���ȼ�ϵ�ص��ܷ�Ӧ����ʽ�ж�pH�ı仯��
��� �⣺��1��CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-890��.3kJ•mol-1���õ�����ϸ��ʹ1mol��������CO2������Һ̬ˮ�ų�����������890��.3kJ•mol-1��
�ʴ�Ϊ��=��
��2���ټ�����CO2�����ںϳɺϳ�������Ҫ�ɷ���һ����̼����������CH4+CO2�T2CO+2H2��1g CH4��ȫ��Ӧ���ͷ�15.46kJ������������1mol������ȫ��Ӧ�ų�������=15.46KJ��16=247.36KJ����Ӧ�ʱ��H=-247.36KJ/mol����ӦΪ���ȷ�Ӧ����Ӧ�����������������Ӧ���Ȼ�ѧ����ʽΪ��CH4��g��+CO2��g���T2CO��g��+2H2��g������H=-247.36KJ/mol�����������仯��ͼ��ֻ��D���ϣ�
�ʴ�Ϊ��D��
�ڷ�Ӧ���Ȼ�ѧ����ʽΪ��CH4��g��+CO2��g���T2CO��g��+2H2��g������H=-247.36KJ/mol��ͼ���֪��Ӧ�ﵽƽ��״̬�ų�����155.80KJ����Ӧ�ļ������ʵ���=$\frac{155.80KJ}{247.36KJ/mol}$=0.63mol������ת����Ϊ63%��
�ʴ�Ϊ��63%��
��3����֪����CH4��g��+2O2��g��=CO2��g��+2H2O��l������H1=-890.3kJ/mol��
��2H2��g��+O2��g���T2H2O��l����H=-571.6kJ•mol-1
��C��s��+O2��g��=CO2��g������H2=-393.5kJ/mol
��˹���ɼ��㣬��+��-�ٵõ�����ӦC��ʯī��s��+2H2��g��=CH4��g����H=-74.8 kJ•mol-1��
�ʴ�Ϊ��-74.8 kJ•mol-1��
��4�����ټ��Լ���ȼ�ϵ����ͨ������һ��aΪԭ��صĸ������ü�����ȼ�Ϸ���ʧ���ӵ�������Ӧ��ͨ��������һ��Ϊԭ��ص������������õ��ӵĻ�ԭ��Ӧ����O2+2H2O+4e-=4OH-���ʴ�Ϊ��a��O2+2H2O+4e-=4OH-��
���ڼ�����Һ�У�����ȼ�ϵ�ص��ܷ�ӦʽΪCH4+2O2+2OH-=CO32-+3H2O����ع���һ��ʱ����������������ӱ����ģ����Ե������Һ��pH���С��
�ʴ�Ϊ����С��
���� ���⿼�����Ȼ�ѧ����ʽ��д����˹���ɼ��㡢��Ӧ������Դ��ȼ�ϵ�ع���ԭ����Ϊ��Ƶ���㣬�������ʵ����ʡ���Ӧ�е������仯����������ԭ�ĽǶ��ж�ԭ��ص��������Լ��缫����ʽ����дΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע�⻯ѧ�о������Ŀ����Է�������Ŀ�Ѷ��еȣ�

 ��ְٷְټ���ϵ�д�
��ְٷְټ���ϵ�д�| A�� | ����̿���л�ԭ�ԣ������������ζ�� | |
| B�� | ����������������ԣ���������ֽƯ�� | |
| C�� | Al2O3���кܸߵ��۵㣬���������������ռ������ | |
| D�� | FeCl3��Һ����Cu��Ӧ��������ʴ��ӡˢ��·�� |
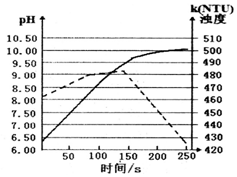 ����ĥ���þ������ʢ��50mL����ˮ���ձ��У���pH���������Ƕȴ����������Һ��pH����Һ�Ƕ���ʱ��ı仯��ͼ�������й�������ȷ�ģ�������
����ĥ���þ������ʢ��50mL����ˮ���ձ��У���pH���������Ƕȴ����������Һ��pH����Һ�Ƕ���ʱ��ı仯��ͼ�������й�������ȷ�ģ�������| A�� | ��ʵ�����ڳ����½��е� | |
| B�� | ʵ�߱�ʾ��Һ�Ƕ���ʱ��ı仯 | |
| C�� | 50sʱ����Һ�е����̪��Һ����Һ��� | |
| D�� | 150s����Һ�Ƕ��½�����Ϊ���ɵ�Mg��OH��2���� |
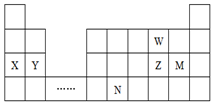
| A�� | ԭ�Ӱ뾶��Y��Z��W�������Ӱ뾶��M-��Z2-��W2- | |
| B�� | ���ʵĻ�ԭ�ԣ�X��Y�����⻯��ķе㣺Z��W | |
| C�� | ����Ԫ��Mͬ���壬����������ˮ��������Ա�M��ǿ | |
| D�� | Ԫ��Nλ�ڽ�����ǽ����ķֽ��߸����������ƶ�N�ĵ��ʿ��� �뵼����� |
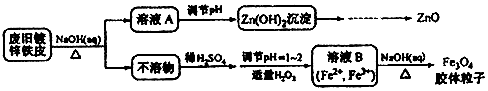
��֪��Zn���仯�����������Al���仯������������ƣ��������˵��������ǣ�������
| A�� | ��NaOH��Һ�����Ͼɶ�п��Ƥ��������ȥ�����ۡ��ܽ��п�� | |
| B�� | ������ҺA��pH����Zn��OH��2�����������ˡ�ϴ�ӡ����ռ����Ƶ�ZnO | |
| C�� | ����ҺB�Ƶ�Fe3O4�������ӵĹ����У������ͨN2����ԭ���Ƿ�ֹFe2+������ | |
| D�� | Fe3O4�����������ü�ѹ���˷�ʵ�ֹ�Һ���� |

| A�� | �����÷�Ӧһ����Ҫ���Ȼ��ȼ������ | |
| B�� | E1�淴Ӧ�Ļ�ܣ�E2������Ӧ�Ļ�� | |
| C�� | �����ܼ�СE1��E2�������ı䷴Ӧ���ʱ� | |
| D�� | X��Y��Z��ʾ�ķ�Ӧ����֮��Ϊ2��1��1 |

 ʳ�����ճ��������Ʒ��Ҳ����Ҫ�Ļ���ԭ�ϣ�
ʳ�����ճ��������Ʒ��Ҳ����Ҫ�Ļ���ԭ�ϣ�