题目内容
15. 1-溴丙烷是一种重要的有机合成中间体,沸点为71℃,密度为1.36g•cm-3.实验室制备少量1-溴丙烷的主要步骤如下:
1-溴丙烷是一种重要的有机合成中间体,沸点为71℃,密度为1.36g•cm-3.实验室制备少量1-溴丙烷的主要步骤如下:步骤1:在仪器A中加入搅拌磁子、12g正丙醇及20mL水,冰水冷却下缓慢加入28mL浓H2SO4;冷却至室温,搅拌下加入24g NaBr.
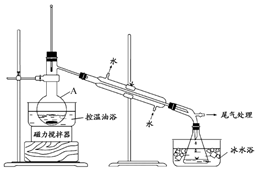
步骤2:如图所示搭建实验装置,缓慢加热,直到无油状物馏出为止.
步骤3:将馏出液转入分液漏斗,分出有机相.
步骤4:将分出的有机相转入分液漏斗,依次用12mL H2O、12mL 5% Na2CO3溶液和12mL H2O洗涤,分液,得粗产品,进一步提纯得1-溴丙烷.
(1)仪器A的名称是蒸馏烧瓶;加入搅拌磁子的目的是搅拌和防止暴沸.
(2)反应时生成的主要有机副产物有2-溴丙烷和丙烯、正丙醚.
(3)步骤2中需向接受瓶内加入少量冰水并置于冰水浴中的目的是减少1-溴丙烷的挥发.
(4)步骤2中需缓慢加热使反应和蒸馏平稳进行,目的是减少HBr挥发.
(5)步骤4中用5%Na2CO3溶液洗涤有机相的操作:向分液漏斗中小心加入12mL 5% Na2CO3溶液,振荡,将分液漏斗下口向上倾斜、打开活塞排出气体,静置,分液.
分析 (1)由图可知仪器的名称,搅拌磁子除搅拌外,还可防止液体剧烈沸腾;
(2)正丙醇在浓硫酸作用下可能发生消去反应,或分子间取代反应;
(3)冰水浴可降低温度,减少生成物的挥发;
(4)步骤2中需缓慢加热,可减少浓硫酸与NaBr反应生成的HBr挥发;
(5)加入12mL 5% Na2CO3溶液,振荡,洗涤1-溴丙烷时可能发生HBr与碳酸钠的反应生成气体,需要排出气体.
解答 解:(1)由图可知,仪器A的名称是蒸馏烧瓶,加入搅拌磁子的目的是搅拌和防止暴沸,
故答案为:蒸馏烧瓶;防止暴沸;
(2)正丙醇在浓硫酸作用下可能发生消去反应,或分子间取代反应,则反应时生成的主要有机副产物有2-溴丙烷和丙烯、正丙醚,
故答案为:丙烯、正丙醚;
(3)步骤2中需向接受瓶内加入少量冰水并置于冰水浴中的目的是减少1-溴丙烷的挥发,
故答案为:减少1-溴丙烷的挥发;
(4)步骤2中需缓慢加热使反应和蒸馏平稳进行,目的是减少HBr挥发,
故答案为:减少HBr挥发;
(5)步骤4中用5%Na2CO3溶液洗涤有机相的操作:向分液漏斗中小心加入12mL 5% Na2CO3溶液,振荡,将分液漏斗下口向上倾斜、打开活塞排出气体,静置,分液,
故答案为:将分液漏斗下口向上倾斜、打开活塞排出气体.
点评 本题考查有机物的制备实验,为高频考点,把握有机物的性质、实验操作及技能为解答的关键,侧重分析能力和实验能力的考查,注意(5)为解答的难点,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列有关水处理方法不正确的是( )
| A. | 用石灰、碳酸钠等碱性物质处理废水中的酸 | |
| B. | 用可溶性的铝盐和铁盐处理水中的悬浮物 | |
| C. | 用氯气处理水中的Cu2+、Hg2+等重金属离子 | |
| D. | 用烧碱处理含高浓度NH4+的废水并回收利用氨 |
6.根据元素周期律和物质结构的有关知识,以下有关排序错误的是( )
| A. | 第一电离能:C<O<N | B. | 电负性:C>N>O | ||
| C. | 热稳定性:HF>H2O>H2S | D. | 酸性:HCl<HBr<HI |
3.下列有关物质的性质与用途具有对应关系的是( )
| A. | 活性炭具有还原性,可用作冰箱除味剂 | |
| B. | 二氧化硫具有氧化性,可用作造纸漂白剂 | |
| C. | Al2O3具有很高的熔点,可用于制造熔融烧碱的坩埚 | |
| D. | FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板 |
12.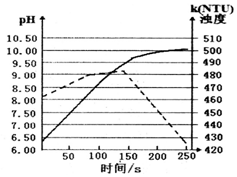 将打磨后的镁条放入盛有50mL蒸馏水的烧杯中,用pH传感器和浊度传感器监测溶液中pH和溶液浊度随时间的变化如图.下列有关描述正确的( )
将打磨后的镁条放入盛有50mL蒸馏水的烧杯中,用pH传感器和浊度传感器监测溶液中pH和溶液浊度随时间的变化如图.下列有关描述正确的( )
 将打磨后的镁条放入盛有50mL蒸馏水的烧杯中,用pH传感器和浊度传感器监测溶液中pH和溶液浊度随时间的变化如图.下列有关描述正确的( )
将打磨后的镁条放入盛有50mL蒸馏水的烧杯中,用pH传感器和浊度传感器监测溶液中pH和溶液浊度随时间的变化如图.下列有关描述正确的( )| A. | 该实验是在常温下进行的 | |
| B. | 实线表示溶液浊度随时间的变化 | |
| C. | 50s时向溶液中滴入酚酞试液,溶液变红 | |
| D. | 150s后溶液浊度下降是因为生成的Mg(OH)2沉降 |
10.在给定的条件下,下列选项所示的物质间转化均能实现的是( )
| A. | FeS2$\stackrel{O_{2}/高温}{→}$SO2$\stackrel{H_{2}O_{2}(aq)}{→}$H2SO4 | |
| B. | Cu2(OH)2CO3$\stackrel{H_{2}SO_{4}}{→}$CuSO4(aq)$\stackrel{Na}{→}$Cu | |
| C. | MgCl2(aq)$\stackrel{△}{→}$MgCl2(s)$\stackrel{电解}{→}$Mg | |
| D. | 1mol•L-1HCl(aq)$\stackrel{MnO_{2}/△}{→}$Cl2$\stackrel{石灰乳}{→}$Ca(ClO)2 |


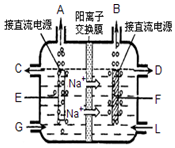 食盐是日常生活必需品,也是重要的化工原料.
食盐是日常生活必需品,也是重要的化工原料.