题目内容
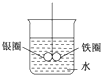 如图所示的装置,在铁圈和银圈的焊接处,用一根棉线将其悬吊在盛水的烧杯中,使之平衡.小心地向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是( )
如图所示的装置,在铁圈和银圈的焊接处,用一根棉线将其悬吊在盛水的烧杯中,使之平衡.小心地向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是( )| A、铁圈和银圈左右摇摆不定 |
| B、保持平衡状况 |
| C、银圈向下倾斜 |
| D、铁圈向下倾斜 |
考点:铁的化学性质
专题:几种重要的金属及其化合物
分析:铁圈和银圈连接浸入硫酸铜溶液中,该装置构成了原电池,较活泼的金属作负极,较不活泼的金属作正极,根据正负极上发生的电极反应判断反应现象.
解答:
解:铁圈和银圈连接浸入硫酸铜溶液中,该装置构成了原电池,较活泼的金属作负极,较不活泼的金属作正极,负极上铁失电子生成亚铁离子进入溶液,所以铁圈质量减少;银圈上铜离子得电子生成铜单质附着在银圈上,导致银圈质量增加,所以观察到的现象是:银圈向下倾斜.
故选C.
故选C.
点评:本题以铁的化学性质考查了原电池原理,为高频考点,题目难度不大,把握铁圈、银圈相连与原电池原理即可解答.

练习册系列答案
相关题目
对于密闭容器中的反应C(s)+02(g)=C02(g),下列说法不正确的是( )
| A、升高温度可以增大化学反应速率 |
| B、将木炭粉碎成粉末可以加快反应速率 |
| C、增大压强可以增大化学反应速率 |
| D、增大炭的用量可以加快反应速率 |
科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:NaHCO3+H2
HCOONa+H2O,下列有关说法正确的是( )
| ||
| 释氢 |
| A、储氢过程中,NaHCO3被氧化 |
| B、释氢过程中,每消耗0.1mol H2O可放出2.24L的H2 |
| C、储氢、释氢过程均无能量变化 |
| D、NaHCO3、HCOONa均含有离子键和共价键 |
前四周期元素X、Y、Z、W、Q的原子序数依次增大.X与Y同周期相邻的非金属元素,Y的基态原子s电子数与p电子数相等,Z是地壳中含量最多的金属元素,W的价电子排布为4s1,基态Q原子的未成对电子是同周期元素中最多的.下列说法错误的是( )
| A、简单氢化物的热稳定性:Y>X |
| B、简单离子的半径:Z>X>Y |
| C、Z的最高价氧化物对应水化物既能与强酸反应又能与强碱反应生产盐和水 |
| D、由Y、W、Q三种元素形成的某种化合物,可用于检查司机酒后驾车 |
常温常压下,将x mol CO2气体通入1L y mol/L的NaOH溶液中,下列对所得溶液的描述不正确的( )


| A、当x=2y时,随着CO2气体的通入,溶液中由水电离出的c(H+)有如图变化关系 | ||||
| B、当x=y时,所得溶液中存在:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) | ||||
| C、当2x=y时,所得溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) | ||||
D、当
|