题目内容
科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:NaHCO3+H2
HCOONa+H2O,下列有关说法正确的是( )
| ||
| 释氢 |
| A、储氢过程中,NaHCO3被氧化 |
| B、释氢过程中,每消耗0.1mol H2O可放出2.24L的H2 |
| C、储氢、释氢过程均无能量变化 |
| D、NaHCO3、HCOONa均含有离子键和共价键 |
考点:氧化还原反应,化学键
专题:氧化还原反应专题,化学键与晶体结构
分析:NaHCO3+H2
HCOONa+H2O中,H元素的化合价升高,C元素的化合价降低,NaHCO3、HCOONa均为离子化合物,且含共价键,以此来解答.
| ||
| 释氢 |
解答:
解:A.C元素的化合价降低,则储氢过程中,NaHCO3被还原,故A错误;
B.释氢过程中,每消耗0.1mol H2O可放出0.1molH2,但状况未知,不能计算其体积,故B错误;
C.该转化为化学变化,一定伴随能量变化,故C错误;
D.NaHCO3、HCOONa均含有钠离子与阴离子形成的离子键和非金属元素形成的(如C-O)共价键,故D正确;
故选D.
B.释氢过程中,每消耗0.1mol H2O可放出0.1molH2,但状况未知,不能计算其体积,故B错误;
C.该转化为化学变化,一定伴随能量变化,故C错误;
D.NaHCO3、HCOONa均含有钠离子与阴离子形成的离子键和非金属元素形成的(如C-O)共价键,故D正确;
故选D.
点评:本题考查氧化还原反应和化学键,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,选项B为易错点,题目难度不大.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A、0.5NA个H2所占的体积约为11.2L |
| B、1 mol OH-所含的电子数为9NA |
| C、标准状况下,9g H2O所占的体积约为11.2L |
| D、标准状况下,28 g CO和N2混合气体的体积约为22.4L |
人体中的O2-(超氧离子)粒子对人体有害,能使人过早衰老,这是因为该离子会在人体中释放出氧化性极强的活性氧.医学界使用对人体无害的亚硒酸钠清除人体内的活性氧,这是利用亚硒酸钠的( )
| A、催化性 | B、氧化性 |
| C、还原性 | D、既有氧化性又有还原性 |
根据下面的信息,判断下列叙述中正确的是( )

| A、氢气跟氧气反应生成水的同时释放能量 | ||
| B、氢气跟氧气反应生成水的同时吸收能量 | ||
C、1mol H2跟
| ||
| D、2mol H2(g)跟1mol O2(g)反应生成2mol H2O(g)释放能量490kJ |
分子式为C3H7Cl的同分异构体有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
下列物质互为同分异构体的一组是( )
| A、12C和14C |
| B、NO和NO2 |
C、CH3CH2CH2CH3和 |
| D、CH3COOH和CH3OCH3 |
下列说法正确的是( )
| A、用新制氢氧化铜悬浊液可检验失去标签的乙醇、丙三醇、乙醛、乙酸四瓶无色溶液 |
| B、检验氯乙烷中的氯元素时,可先将氯乙烷硝酸进行酸化,再加硝酸银溶液来检验,通过观察是否有白色沉淀来判断是否存在氯元素 |
| C、摩尔盐制备过程中铁屑要先用碳酸钠溶液浸泡洗涤,使用热的碳酸钠溶液有利提高去油污的能力,最后分离溶液和固体时不可以用倾析法 |
| D、由于苯酚与溴水发生反应时,副反应多,所以只能利用溴水对含苯酚的废水作定性检验,不能用作定量测定 |
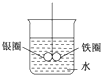 如图所示的装置,在铁圈和银圈的焊接处,用一根棉线将其悬吊在盛水的烧杯中,使之平衡.小心地向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是( )
如图所示的装置,在铁圈和银圈的焊接处,用一根棉线将其悬吊在盛水的烧杯中,使之平衡.小心地向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是( )| A、铁圈和银圈左右摇摆不定 |
| B、保持平衡状况 |
| C、银圈向下倾斜 |
| D、铁圈向下倾斜 |