题目内容
9.化学与社会、生产密切相关,下列说法正确的是( )| A. | 高纯度的单晶硅用于制造光导纤维 | |
| B. | 从海水中提取物质都必须通过化学反应才能实现 | |
| C. | 乙酸乙酯在碱性条件下水解称为皂化反应 | |
| D. | 可溶性铜盐有毒,在生命体中铜是一种不可缺少的微量元素 |
分析 A.光导纤维主要成分是二氧化硅;
B.从海水中可以提取氯化钠为物理过程;
C.皂化反应是特指油脂在碱性条件下水解;
D.铜离子属于重金属离子,可以使蛋白质变性.
解答 解:A.光导纤维主要成分是二氧化硅,不是硅,故A错误;
B.从海水中提取蒸馏水和盐时,通过蒸馏、蒸发等物理变化就能实现,提取溴、碘、镁等物质时,必须通过化学反应才能实现,故B错误;
C.皂化反应是特指油脂在碱性条件下水解,故C错误;
D.可溶性铜盐中含有重金属离子铜离子,重金属离子可以使蛋白质变性,所以说可溶性铜盐有毒;铜与人体健康有着密切的关系,铜是人体健康内一种必需的微量元素,在人体的新陈代谢过程中起着重要的作用,故D正确;
故选:D.
点评 本题考查了化学与生产和生活关系,熟悉二氧化硅的性质、皂化反应的概念、化学变化与物理变化的区别是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.下列有关各实验装置图的叙述中,正确的是( )


| A. | 装置①储存液溴 | B. | 装置②提纯含少量水的乙醇 | ||
| C. | 装置③不能用来吸收HCl气体 | D. | 装置④分离CCl4和水 |
20.已知常温下Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=5×10-13,下列有关说法错误的是( )
| A. | 在饱和AgCl,AgBr的混合溶液中:$\frac{c(C{l}^{-})}{c(B{r}^{-})}$=360 | |
| B. | 向AgCl悬浊液中滴加NaBr溶液会产生淡黄色沉淀 | |
| C. | AgCl在水中溶解度及Ksp均比在NaCl溶液中的大 | |
| D. | 欲用1L NaCl溶液将0.01 mol AgBr转化为AgCl,则c(NaCl)>3.61 mol/L |
17.化学与生产、生活密切相关.下列叙述中正确的是( )
| A. | 用浓H2SO4刻蚀工艺玻璃上的纹饰 | |
| B. | 高纯度的硅单质广泛用于制作光导纤维 | |
| C. | 漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 | |
| D. | 制饭勺、饭盒、高压锅等的不锈钢是合金 |
4.已建立化学平衡的某可逆反应,当改变条件使平衡向正反应方向移动,正确的是( )
| A. | 生成物的百分含量一定增加 | B. | 正反应速率大于逆反应速率 | ||
| C. | 反应物的转化率一定增大 | D. | 反应物浓度一定降低 |
1.下列关系式中,正确的是( )
| A. | 等浓度等体积的CH3COOH和CH3COONa溶液混合:c(CH3COO-)+c(OH-)=c(H+)+c(CH3COOH) | |
| B. | 常温下,0.1 mol•L-1HA溶液与0.1 mol•L-1NaOH溶液等体积完全反应时,溶液中一定存在:c(Na+)=c(A-)>c(OH-)=c(H+) | |
| C. | 常温下,0.1 mol•L-1Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| D. | 常温下,将0.1 mol•L-1 CH3COOH溶液加水稀释,当溶液的pH从3.0升到5.0时,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$的值增大到原来的100倍 |
18. 恒容容器中,对于可逆反应xX(g)+yY(g)?zZ(g)+mM(g),x的百分含量随时间的变化如图,下列说法正确的是( )
恒容容器中,对于可逆反应xX(g)+yY(g)?zZ(g)+mM(g),x的百分含量随时间的变化如图,下列说法正确的是( )
 恒容容器中,对于可逆反应xX(g)+yY(g)?zZ(g)+mM(g),x的百分含量随时间的变化如图,下列说法正确的是( )
恒容容器中,对于可逆反应xX(g)+yY(g)?zZ(g)+mM(g),x的百分含量随时间的变化如图,下列说法正确的是( )| A. | x+y>z+m | |
| B. | 对反应体系加压v正>v逆 | |
| C. | 该反应正反应方向为热反应 | |
| D. | 对反应体系降低温度达平衡前v逆>v正 |
19.下列式子表示的物质一定为纯净物的是( )
| A. | C2H6O | B. | CH4O | C. | C2H4O2 | D. | C7H16 |
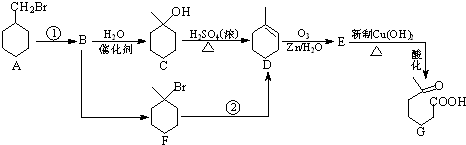

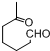 +NaOH+2Cu(OH)2$\stackrel{△}{→}$
+NaOH+2Cu(OH)2$\stackrel{△}{→}$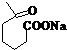 +Cu2O↓+3H2O;
+Cu2O↓+3H2O; 物质D与呋喃(
物质D与呋喃( )也可以发生“Diels-Alder反应”,该化学反应方程式为
)也可以发生“Diels-Alder反应”,该化学反应方程式为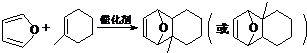 .
.