题目内容
4.设NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 1L水中溶解5.85gNaCl所形成溶液物质的量浓度是0.1mol•L-1 | |
| B. | 46gNO2和N2O4混合气体中含有原子总数为3NA | |
| C. | 标准状况下,22.4L单质溴所含有的原子数目为2NA | |
| D. | 3.4gNH3中含N-H键数目为0.2NA |
分析 A、当氯化钠溶于1L水中后,溶液体积大于1L;
B、NO2和N2O4的最简式均为NO2;
C、标况下单质溴为液态;
D、求出氨气的物质的量,然后根据1mol氨气中含3molN-H键来分析.
解答 解:A、当氯化钠溶于1L水中后,溶液体积大于1L,故溶液的物质的量浓度小于0.1mol/L,故A错误;
B、NO2和N2O4的最简式均为NO2,故46g混合物中含有的NO2的物质的量为1mol,故含3NA个原子,故B正确;
C、标况下单质溴为液态,故不能根据气体摩尔体积来计算其物质的量和原子个数,故C错误;
D、3.4g氨气的物质的量为0.2mol,而1mol氨气中含3molN-H键,故0.2mol氨气中含0.6NA条N-H键,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
12.下列有机物有顺反异构体的是( )
| A. | CH3CH3 | B. | CH2=CH2 | C. | CH3CH=CHCl | D. | CH3CH=CH2 |
19.下列说法中,正确的是( )
| A. | 仅由碳元素组成的物质一定是纯净物 | |
| B. | 金刚石、石墨、足球烯(C60)互为同素异形体 | |
| C. | 同素异形体之间的转化属于物理变化 | |
| D. | 金刚石和石墨的性质完全相同 |
9.下列叙述不正确的是( )
| A. | H2S与SO2、NO与O2、NH3与HCl在常温下均不能大量共存 | |
| B. | (NH4)2SO3、Ca(HCO3)2、NaAlO2均既能和稀硫酸又能和氢氧化钠溶液反应 | |
| C. | Fe(OH)3、FeCl2、FeCl3均可通过化合反应得到 | |
| D. | 制备Fe(OH)2时加苯液封,同时将滴管插入苯层液面以下,其目的是防止Fe(OH)2被空气氧化 |
13.下列有关说法正确的是( )
| A. | Hg(l)+H2SO4(aq)=HgSO4(aq)+H2(g)常温下不能自发进行,说明△H<0 | |
| B. | 在一密闭容器中发生2SO2(g)+O2(g)?2SO3(g)反应,平衡后增大压强,平衡会正向移动,$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})•c({O}_{2})}$值增大 | |
| C. | 已知25℃时,Ksp(AgCl)=1.8×10-10、Ksp(Ag2CrO4)=2.0×10-12,所以AgCl的溶解度大于Ag2CrO4的溶解度 | |
| D. | 向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进了Fe3+水解 |
14.下列各组物质的晶体中,化学键类型完全相同、晶体类型也相同的是( )
| A. | CO2和SiO2 | B. | NaCl和HCl | C. | H2O和H2 | D. | KOH和KCl |
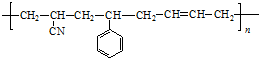 除苯乙烯外,还需要另外两种单体,写出这两种单体的结构简式CH2=CH-CN、CH2=CH-CH=CH2.
除苯乙烯外,还需要另外两种单体,写出这两种单体的结构简式CH2=CH-CN、CH2=CH-CH=CH2.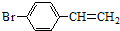 )需要三步,第一步选用的试剂为HBr,目的是保护碳碳双键防止被加成.
)需要三步,第一步选用的试剂为HBr,目的是保护碳碳双键防止被加成.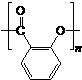 .
.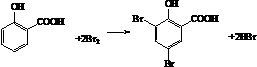 .
.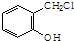 制备A的合成路线
制备A的合成路线