题目内容
7.下列有关性质的比较,不能用元素周期律解释的是( )| A. | 非金属性:Cl>Br | B. | 酸性:H2SO3>H2CO3 | ||
| C. | 碱性:KOH>NaOH | D. | 热稳定性:NH3>PH3 |
分析 A.周期元素从左到右,非金属性依次减弱;
B.亚硫酸不是最高价含氧酸;
C.元素的金属性越强,对应的最高价氧化物的水化物的碱性越强;
D.非金属性越强,对应氢化物的稳定性越强.
解答 解:A.周期元素从左到右,非金属性依次减弱,则非金属性:Cl>S,能用元素周期律解释,故A不选;
B.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,H2SO3不是最高价含氧酸,不能用元素周期律解释,故B选;
C.元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,金属性:Na>Mg,则碱性:NaOH>Mg(OH)2,能用元素周期律解释,故C不选;
D.非金属性越强,对应氢化物稳定性越强,非金属性N>P,则热稳定性:NH3>PH3,能用元素周期律解释,故D不选;
故选B.
点评 本题考查了原子结构与元素周期律的应用,题目难度不大,注意把握元素周期律的递变规律以及相关知识的积累,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
17.下列关于燃料充分燃烧的说法中,错误的是( )
| A. | 氧气量充足,燃烧充分 | B. | 固体燃料块越大燃烧越充分 | ||
| C. | 液体燃料燃烧时可以雾状喷出 | D. | 温度必须达到着火点 |
18.近年来我国加强了稀土资源的保护.铈(Ce)是一种稀土元素,它的一种核素中含有58个质子和80个中子,则其表示为( )
| A. | ${\;}_{58}^{80}$Ce | B. | ${\;}_{58}^{138}$Ce | C. | ${\;}_{80}^{58}$Ce | D. | ${\;}_{80}^{138}$Ce |
15.25℃时,水的电离达到平衡:H2O?H++OH-△H>0,下列叙述正确的是( )
| A. | 向平衡体系中加入水,平衡正向移动,c (H+)增大 | |
| B. | 将水加热,Kw增大,pH不变 | |
| C. | 向水中加入少量硫酸氢钠固体,$\frac{c({H}^{+})}{c(O{H}^{-})}$增大 | |
| D. | 向水中加入少量NaOH固体,平衡正向移动,c(H+)降低 |
2.用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新技术.已知反应Fe2O3+3Na2O2$\frac{\underline{\;熔融\;}}{\;}$2Na2FeO4+Na2O,下列说法不正确的是( )
| A. | 该反应中Na2O2既是氧化剂又是还原剂 | |
| B. | Na2FeO4既是氧化产物又是还原产物 | |
| C. | 1mol Na2O2发生反应,有2mol电子转移 | |
| D. | 在Na2FeO4中Fe为+6价,具有强氧化性,能消毒杀菌 |
12.在密闭容器中进行如下反应:X2(g)+Y2(g)?2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A. | X2为0.2mol/L | B. | Y2为0.2mol/L | C. | Z为0.3mol/L | D. | Z为0.45mol/L |
19.鉴别CII3OCH3和CH3CH2OH可采用化学方法和物理方法,下列方法不能对二者进行鉴别的是( )
| A. | 利用金属钠或金属钾 | B. | 利用质谱法 | ||
| C. | 利用红外光谱 | D. | 利用核磁共振氢谱 |
1.亚硫酰氯(SOCl2)是一种液态化合物,沸点770C.是一种重要的化工产品.加热可发生反应4SOCl2$\frac{\underline{\;200℃左右\;}}{\;}$2SO2+S2Cl2+3Cl2(S2Cl2的沸点为138X:).工业上合成亚硫酰氯方法之一是:
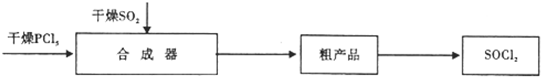
已知:合成器中发生的反应为:PCl5(熔融)+SO2$\frac{\underline{\;一定温度\;}}{\;}$SOCl2+POCl3△H<0 (POCl3 的沸点为105.3℃)
请回答下列问题:
(1)要得到干燥的SO2气体,可将潮湿的SO2通过装有AD的干燥装置(填写字母番号,多选).
A.浓硫酸B.生石灰C.氢氧化钠D.硅胶
(2)工业上从粗产品中,可采用分馏(或蒸馏)的方法(填写操作方法)获得较纯的SOCl2.
(3)合成器的内层,最好选用耐高温、耐氧化、耐腐蚀(工程陶瓷或耐高温陶瓷)材料制成.
(4)已知SOCl2与H2OI发生剧烈反应,有白雾形成并逸出有剌激性气味的气体,请写出该 反应的化学方程式SOCl2+H2O=SO2↑+HCl↑.
(5)SOCl2已Li-SOCl2电池,其电极材料分别为锂和碳,电解液是LiAlCl-SOCl2.电池的总反应可表示为:Li+SOCl2═4LiCl+S+SO2.该电池的负极的电极反应式为Li-e-=Li+
(6)某学习小组用刚吸收过少量SO2的NaOH溶液吸收SOOl2加热分解并冷却至室温后 的气体.吸收一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO${\;}_{4}^{2-}$.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中的CO2的影响).
①提出合理假设.
假设1:只存在SO${\;}_{3}^{2-}$;假设2:既不存在SO${\;}_{3}^{2-}$也不存在ClO-;假设3:只存在ClO-.
②设计实验方案,进行实验.请写出实验步骤以及预期现象和结论.限选实验试剂:3moL.L-1H2SO4溶液、1moL.L-1NaOH溶液、0.1moL.L-1KMnO4溶液、淀粉一KI溶液、紫色石蕊试液.

已知:合成器中发生的反应为:PCl5(熔融)+SO2$\frac{\underline{\;一定温度\;}}{\;}$SOCl2+POCl3△H<0 (POCl3 的沸点为105.3℃)
请回答下列问题:
(1)要得到干燥的SO2气体,可将潮湿的SO2通过装有AD的干燥装置(填写字母番号,多选).
A.浓硫酸B.生石灰C.氢氧化钠D.硅胶
(2)工业上从粗产品中,可采用分馏(或蒸馏)的方法(填写操作方法)获得较纯的SOCl2.
(3)合成器的内层,最好选用耐高温、耐氧化、耐腐蚀(工程陶瓷或耐高温陶瓷)材料制成.
(4)已知SOCl2与H2OI发生剧烈反应,有白雾形成并逸出有剌激性气味的气体,请写出该 反应的化学方程式SOCl2+H2O=SO2↑+HCl↑.
(5)SOCl2已Li-SOCl2电池,其电极材料分别为锂和碳,电解液是LiAlCl-SOCl2.电池的总反应可表示为:Li+SOCl2═4LiCl+S+SO2.该电池的负极的电极反应式为Li-e-=Li+
(6)某学习小组用刚吸收过少量SO2的NaOH溶液吸收SOOl2加热分解并冷却至室温后 的气体.吸收一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO${\;}_{4}^{2-}$.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中的CO2的影响).
①提出合理假设.
假设1:只存在SO${\;}_{3}^{2-}$;假设2:既不存在SO${\;}_{3}^{2-}$也不存在ClO-;假设3:只存在ClO-.
②设计实验方案,进行实验.请写出实验步骤以及预期现象和结论.限选实验试剂:3moL.L-1H2SO4溶液、1moL.L-1NaOH溶液、0.1moL.L-1KMnO4溶液、淀粉一KI溶液、紫色石蕊试液.
| 实验步骤 | 预期现象和结论 |
| 步骤1取少量吸收液于试管中滴加3moL.L-1H2SO4,至溶液呈酸性,然后将所得溶液分置于A、B试管中. | 无明显现象 |
| 步骤2:在A试管中滴加紫色石蕊试液 | 若先变红后褪色,证明有ClO-,否则无 |
| 步骤3:在B试管中滴加0.01mol•L-1KMnO4溶液 | 若紫红色褪去,证明有SO32-,否则无 |
2.常温下,某溶液X由Fe3+、SO42-、Cu2+、Na+、CO32-、Al3+中的几种离子组成.取少量待测液滴加KSCN溶液,溶液变红;另取少量待测滴加NaOH溶液至pH=4后过滤,向滤液中继续滴加NaOH溶液至过量时又得到沉淀W和溶液Y.可能用到的数据如下表所示,下列说法正确的是( )
| 沉淀物 | Fe(OH)3 | Cu(OH)2 | Al(OH)3 |
| 开始沉淀的pH | 1.9 | 4.7 | 3.4 |
| 沉淀完全的pH | 3.2 | 6.7 | 4.7 |
| A. | 该温度下Ksp[Fe(OH)3]=1×10-14.6 | |
| B. | W主要含有 Cu(OH)2和Al(OH)3 | |
| C. | 溶液X中一定含有Cu2+、Fe3+和SO42- | |
| D. | 取溶液Y进行焰色反应,可判断溶液X中是否含有Na+ |